Farmaci
I nuovi farmaci dimagranti pongono seri rischi per le donne incinte

Renovatio 21 traduce questo articolo per gentile concessione di Children’s Health Defense. Le opinioni degli articoli pubblicati non coincidono necessariamente con quelle di Renovatio 21.
La Food and Drug Administration degli Stati Uniti avverte che Ozempic – approvato per il diabete ma usato off label per la perdita di peso – e Wegovy dovrebbero essere interrotti almeno due mesi prima della gravidanza, ma questi avvertimenti sono sepolti e i test a lungo termine non saranno completati per anni.
Ozempic e Wegovy, i farmaci al centro dell’ultima mania per la perdita di peso, comportano rischi seri e poco discussi per le donne incinte.
La Food and Drug Administration (FDA) statunitense avverte che l’uso di Ozempic – approvato per il diabete ma usato off label per la perdita di peso – e Wegovy dovrebbe essere interrotto almeno due mesi prima della gravidanza perché il corpo impiega così tanto tempo per eliminare la droga.
Tuttavia il National Institutes of Health (NIH) riferisce che quasi la metà delle gravidanze negli Stati Uniti non sono pianificate. E il farmaco è popolare tra le donne e commercializzato a donne in età fertile.
Gli effetti collaterali dei farmaci per le donne incinte non sono chiari nel marketing, la neuroscienziata Martha Bagnell, Ph.D. , ha detto a Vox. «Data la prevalenza di pubblicità Ozempic con donne in essa», ha detto, «penseresti che sia un effetto collaterale piuttosto grande su cui attirare l’attenzione».
Ozempic e Wegovy sono nomi brandizzati per il semaglutide, un agonista del GLP-1 che riduce l’assunzione di cibo frenando l’appetito e rallentando la digestione. I farmaci vengono assunti tramite iniezioni settimanali autosomministrate.
Quando la FDA ha approvato Wegovy per la perdita di peso nel 2021, ha richiesto al produttore del farmaco, Novo Nordisk, di condurre studi post-marketing di follow-up sugli esiti di salute delle donne incinte, dei loro feti e dei neonati esposti al farmaco durante la gravidanza.
Nessuno dei due farmaci è stato studiato nelle donne in gravidanza negli studi clinici. Ma negli studi sugli animali, quando ratti, conigli e scimmie sono stati trattati con farmaci semaglutide iniettabili, hanno sperimentato un aumento dei tassi di aborto spontaneo e la loro prole è nata più piccola e ha avuto tassi di difetti alla nascita più elevati di quanto normalmente previsto.
«Dovrebbero davvero avere un black box warning»
Sepolto nell’etichetta del farmaco Ozempic di 44 pagine e nell’etichetta del farmaco Wegovy di 34 pagine, Novo Nordisk afferma che ci sono dati limitati sull’uso di semaglutide nelle donne in gravidanza – perché non ci sono stati studi clinici – ma che gli studi sugli animali in gravidanza indicano che ci sono potenziali rischi per il feto derivanti dall’esposizione al farmaco durante la gravidanza.
Entrambe le etichette si basano sugli stessi studi, che mostrano danni ai feti di ratti, conigli e scimmie che hanno ricevuto farmaci semaglutide durante la gravidanza.
I ricercatori hanno riscontrato mortalità embrio-fetale, nati morti e «anomalie strutturali» quando alle madri veniva somministrata semaglutide al di sotto della dose umana massima raccomandata.
Gli studi sugli animali hanno anche rilevato una crescita ridotta, anomalie dei vasi sanguigni del cuore e dello scheletro e aborti spontanei a livelli di esposizione umana.
Anche gli animali in allattamento avevano il farmaco nel latte materno.
Ozempic, dice l’etichetta, dovrebbe quindi «essere usato durante la gravidanza solo se il potenziale beneficio giustifica il potenziale rischio per il feto». Wegovy, la versione più forte di semaglutide, afferma che quando viene scoperta la gravidanza, l’uso dovrebbe interrompersi.
«Questo è uno scenario terrificante, come un enorme treno merci che scende dai binari del treno che non sarai in grado di fermare», ha detto a The Defender il dottor James Thorp, un ostetrico e ginecologo certificato.
«Il problema è che l’intero settore viene catturato. Alcune persone lo definiscono un farmaco miracoloso e molte donne si stanno riversando su di esso. Ciò significa che stanno spingendo questi farmaci alla popolazione esatta che avrà gravidanze involontarie. Quindi questo è un disastro» ha affermato.
Thorp, che è anche uno specialista in medicina materno-fetale certificato dal consiglio di amministrazione con oltre 40 anni di esperienza, ha affermato che i farmaci «dovrebbero davvero avere un black box warning [un tipo di avvertenza che appare sul foglietto illustrativo di alcuni farmaci soggetti a prescrizione medica, così chiamato perché l’ente regolatore del farmaco americano FDA specifica che è formattato con una «casella» o un bordo intorno al testo per sottolineare l’eventuale pericolo, ndt] per il rischio di gravidanza. Perché quando lo pubblichi nella popolazione generale, ci saranno donne che lo prenderanno e finiranno per ferire una gravidanza».
I black box warning sono il tipo di avvertimento più serio usato dalla FDA.
Ozempic e Wegovy hanno incluso avvertimenti sulla gravidanza ma li hanno sepolti nelle istruzioni, in fondo all’elenco dei possibili effetti collaterali.
La FDA ha detto a Vox che l’agenzia avrebbe reso più importante un avviso di gravidanza solo se fossero stati osservati eventi teratogeni – anomalie fetali dovute all’esposizione al farmaco che di solito vengono scoperte dopo una maggiore prevalenza di un particolare difetto alla nascita, simile a quanto accaduto con la talidomide negli anni ’60.
La FDA ha anche detto a Vox che «l’agenzia ritiene che le complicazioni della gravidanza siano probabilmente causate dalla perdita di peso e da una cattiva alimentazione», il che implica che il problema riguarda la perdita di peso, non il farmaco.
Il portavoce della FDA ha affermato che «l’assunzione di semaglutide durante la gravidanza può aumentare il rischio di difetti alla nascita e aborto spontaneo rispetto allo sfondo per la popolazione generale degli Stati Uniti», ma l’entità dell’aumento del rischio non è stata ancora quantificata, ha riferito Vox.
Secondo la tempistica della FDA per l’approvazione del farmaco dimagrante di Novo Nordisk, l’azienda deve condurre uno studio prospettico che creerà un registro per seguire gli esiti di salute delle donne incinte che assumono Wegovy e confrontare gli esiti materni, fetali e infantili di quelle donne con donne non drogate.
«Il registro rileverà e registrerà malformazioni congenite maggiori e minori, aborti spontanei, nati morti, interruzioni elettive, piccoli per l’età gestazionale, parto pretermine e qualsiasi altro esito negativo della gravidanza».
Ma gli studi non saranno completati prima del 2027 e del 2033.
Nel frattempo, ha detto Thorp, milioni di donne probabilmente assumeranno questi farmaci.
«Questi sono farmaci relativamente nuovi e non abbiamo alcun profilo di sicurezza sulla gravidanza negli esseri umani», ha detto Thorp. «Perché non dovrebbero consigliare le donne in modo più serio sui rischi? Questa è una ricetta per il disastro», ha dichiarato.
Nessuno studio a lungo termine sugli effetti collaterali
Da quando la FDA ha approvato Wegovy, il farmaco è diventato una sensazione, con celebrità e influencer dei social media che condividono regolarmente foto prima e dopo su Instagram e TikTok, contribuendo ad alimentare un nuovo enorme mercato della droga che potrebbe valere 100 miliardi di dollari all’anno per i creatori.
Wegovy era così popolare che c’erano carenze e i pazienti si sono rivolti ad altri prodotti farmaceutici – come Ozempic di Novo Nordisk – che possono essere usati off-label per la perdita di peso e che sono diventati altrettanto popolari.
I produttori di farmaci non sono gli unici a trarre profitto dai farmaci dimagranti. Le società di telemedicina sono sorte online offrendo una prescrizione per i farmaci in soli 15 minuti.
Aziende come Ro e Calibrate hanno lanciato servizi di telemedicina dedicati alla prescrizione di Wegovy e Ozempic e hanno pubblicato annunci per i loro servizi in luoghi come New York City.
La scorsa settimana il valore delle azioni di WW International (precedentemente Weight Watchers) è salito del 46% quando ha annunciato l’acquisizione di una nuova piattaforma di telemedicina, «Sequence», che secondo la società la aiuterà ad entrare nel mercato in forte espansione dei nuovi farmaci per l’obesità – previsto raggiungere i 4,3 miliardi di dollari entro il 2032.
I farmaci hanno causato la perdita di peso negli studi clinici. Gli utenti possono pagare più di 1.300 dollari al mese per i farmaci, che spesso non sono coperti da un’assicurazione per la perdita di peso.
Ma i farmaci non sono fatti per un uso a breve termine: quando le persone smettono di prenderli, recuperano gran parte del peso perso, dimostrano gli studi.
Non ci sono studi a lungo termine sugli effetti dei farmaci. E altri effetti collaterali noti includono pancreatite, cancro alla tiroide, gonfiore della cistifellea, insufficienza renale e retinopatia diabetica.
All’inizio di quest’anno, l’American Association of Pediatrics ha emesso nuove raccomandazioni per l’obesità infantile, consigliando che anche i bambini obesi di appena 8 anni possono essere trattati con farmaci dimagranti, incluso il semaglutide.
La FDA ha inoltre incaricato Novo Nordisk di completare gli studi post-marketing nei bambini di età pari o superiore a 6 anni e per altri gravi effetti collaterali, tra cui carcinoma midollare della tiroide, disturbi del pancreas e della cistifellea, danno renale acuto, gravi eventi epatici, neoplasie maligne, grave ipoglicemia e gravi disturbi gastrointestinali disturbi.
Brenda Baletti
Phd.
Renovatio 21 offre questa traduzione per dare una informazione a 360º. Ricordiamo che non tutto ciò che viene pubblicato sul sito di Renovatio 21 corrisponde alle nostre posizioni.
Farmaci
Wegovy, produttrice di Ozempic, non ha segnalato ictus, ideazione suicidaria e decessi

Renovatio 21 traduce questo articolo per gentile concessione di Children’s Health Defense. Le opinioni degli articoli pubblicati non coincidono necessariamente con quelle di Renovatio 21.
La FDA ha rimproverato Novo Nordisk per «gravi violazioni» relative alla mancata segnalazione di gravi effetti collaterali associati ai suoi farmaci di successo a base di GLP-1, tra cui Ozempic e Wegovy. Gli investigatori hanno affermato che l’azienda non ha segnalato casi di ictus, tendenze suicide e decessi di pazienti, sollevando preoccupazioni circa problemi sistemici nel monitoraggio della sicurezza dei farmaci.
Secondo la Food and Drug Administration (FDA) statunitense, il produttore di diversi farmaci dimagranti di grande successo non ha segnalato gravi effetti collaterali, tra cui ictus, ideazione suicidaria e decessi.
Questo mese la FDA ha inviato una lettera di avvertimento formale a Novo Nordisk, rimproverando il colosso farmaceutico per «gravi violazioni» relative alla mancata segnalazione di gravi effetti collaterali legati a Ozempic, Wegovy e Saxenda.
La lettera del 5 marzo faceva seguito alle ispezioni della FDA, condotte a gennaio e febbraio, presso le attività statunitensi di Novo Nordisk a Plainsboro, nel New Jersey.
Gli inquirenti hanno concluso che l’azienda non ha rispettato le normative federali che regolano la segnalazione degli eventi avversi post-commercializzazione (PADE), un sistema di sicurezza fondamentale utilizzato per individuare segnali di pericolo dopo che i farmaci sono già stati immessi sul mercato.
In base alla legge federale, le aziende farmaceutiche devono segnalare tempestivamente alla FDA tutti i casi gravi di eventi avversi entro 15 giorni dal ricevimento della segnalazione, in modo che le autorità di regolamentazione possano monitorare i rischi emergenti per i consumatori.
Tuttavia, Novo Nordisk, in violazione della legge, ha scelto di non segnalare eventi avversi gravi, tra cui ictus e decessi di pazienti, dopo che il suo personale o i suoi collaboratori esterni avevano stabilito che gli effetti collaterali non erano correlati ai farmaci.
Gli inquirenti hanno scoperto che la casa farmaceutica non ha rispettato alcune delle proprie procedure interne, tra cui l’aver tentato di ottenere informazioni sulla sicurezza in casi gravi di decessi segnalati.
Nella corrispondenza intercorsa con l’agenzia dopo l’ispezione, l’azienda ha dichiarato di aver intrapreso «azioni correttive e preventive» per porre rimedio alle violazioni.
Ciononostante, la FDA ha inviato all’azienda una lettera di avvertimento perché, a suo dire, la risposta di Novo non forniva dettagli sufficienti a dimostrare se tali azioni avrebbero effettivamente risolto i problemi.
Sostieni Renovatio 21
Novo non ha segnalato ideazione suicidaria, decessi e ictus collegati ai farmaci
La lettera della FDA delinea una serie di argomentazioni fallaci utilizzate da Novo per giustificare la mancata segnalazione di diversi eventi.
La lettera descriveva il caso di un paziente che aveva subito un ictus invalidante dopo aver assunto liraglutide (Saxenda). L’azienda non lo aveva segnalato perché, a suo dire, il consumatore non riteneva che l’ictus fosse correlato al farmaco.
In un altro caso, un medico ha segnalato che un paziente in cura con semaglutide si era suicidato. Novo ha scelto di non indagare sul caso.
L’azienda ha segnalato un altro caso di ideazione suicidaria alla FDA solo dopo che gli ispettori dell’agenzia si sono imbattuti nella documentazione mentre indagavano su un decesso per ictus non segnalato.
Studi indipendenti hanno collegato questi farmaci all’ideazione suicidaria.
In un altro caso, Novo ha dichiarato di non aver indagato sul decesso di un paziente correlato a semaglutide (Ozempic, Wegovy) perché l’azienda non aveva ricevuto il consenso dalla persona che aveva segnalato il decesso. Secondo la FDA, il consenso non è richiesto per le indagini PADE (Patient-Related Event).
La FDA ha inoltre riscontrato che, anche dopo aver avvertito Novo che stava violando la legge, i suoi appaltatori hanno continuato a «invalidare in modo improprio» i casi di eventi avversi gravi. L’azienda ha affermato che gli eventi non erano validi perché privi di identificativi del paziente, ovvero informazioni protette, come il nome o il codice fiscale, che collegano una persona alla sua cartella clinica.
Tuttavia, stando alla lettera, gli ispettori della FDA hanno trovato identificativi validi dei pazienti nei documenti originali dei rapporti interni dell’azienda.
Iscriviti alla Newslettera di Renovatio 21
Guasti sistemici che coinvolgono l’intero portafoglio prodotti di Novo.
Questi casi di mancata segnalazione non sono stati eventi isolati. Al contrario, «suggeriscono fallimenti sistemici» nel modo in cui l’azienda riceve, valuta e comunica i dati sulla sicurezza alle autorità federali, ha affermato la FDA.
«In base alla natura dei risultati dell’ispezione e alla vostra risposta scritta e alla corrispondenza, nutriamo serie preoccupazioni circa la portata e l’impatto di queste violazioni sull’intero portafoglio prodotti», ha comunicato la FDA all’azienda.
I dirigenti di Novo hanno difeso l’azienda in una dichiarazione pubblicata sul suo sito web, indicando che «si sta adoperando per risolvere le osservazioni» contenute nella lettera.
«Novo Nordisk prende sul serio i requisiti di segnalazione degli eventi avversi correlati al farmaco e prevediamo di rispondere alle richieste contenute nella lettera di avvertimento in modo rapido e completo», ha dichiarato Anna Windle, responsabile dello sviluppo clinico, degli affari medici e regolatori di Novo Nordisk US.
I sistemi di segnalazione degli eventi avversi sono fondamentali per il monitoraggio della sicurezza dei farmaci. Se i problemi non vengono segnalati tempestivamente e in modo accurato, le autorità di regolamentazione potrebbero non cogliere i segnali precoci di un potenziale danno causato da un farmaco.
Gli esperti di sicurezza dei farmaci avvertono da tempo che i sistemi di sorveglianza post-marketing dipendono fortemente dalle aziende produttrici per la segnalazione accurata dei dati sulla sicurezza, sollevando preoccupazioni circa potenziali conflitti di interesse.
Molte riviste mediche hanno sollecitato una migliore segnalazione degli eventi avversi, soprattutto a seguito di importanti scandali, come il ritiro dal mercato del Vioxx da parte della Merck dopo che aveva causato decine di migliaia di problemi cardiaci e decessi.
Questa settimana la FDA ha lanciato un nuovo sistema per il monitoraggio degli eventi avversi, affermando che migliorerà l’efficienza e la trasparenza. Mentre alcuni hanno accolto con favore il nuovo Sistema di Monitoraggio degli Eventi Avversi (AEMS), alcuni critici hanno sostenuto che il nuovo sistema non risolve tutti i problemi di lunga data dei sistemi che intende sostituire.
La FDA richiede una risposta entro 15 giorni
Le lettere di avvertimento sono tra gli strumenti di controllo più efficaci della FDA, dopo le azioni legali. Notificano alle aziende violazioni normative significative e richiedono l’adozione immediata di misure correttive per evitare ulteriori provvedimenti.
Novo Nordisk dovrà rispondere entro 15 giorni lavorativi fornendo una spiegazione dettagliata delle azioni correttive intraprese.
Se la FDA ritiene che la risposta dell’azienda sia inadeguata, l’agenzia può adottare ulteriori misure coercitive, tra cui multe, sequestri di prodotti o ingiunzioni.
Aiuta Renovatio 21
L’azienda deve affrontare 4.000 cause legali negli Stati Uniti per effetti collaterali che cambiano la vita.
La domanda globale dei farmaci dimagranti di Novo, appartenenti alla classe di farmaci noti come agonisti del recettore GLP-1, è aumentata vertiginosamente negli ultimi anni, alimentata da aggressive campagne di marketing.
Questi farmaci, prodotti anche dalla concorrente di Novo, Eli Lilly, sono diventati tra i prodotti farmaceutici più redditizi al mondo.
I farmaci GLP-1 vengono sempre più spesso presentati come una panacea per problemi che vanno oltre la perdita di peso, includendo una vasta gamma di disturbi, dalla dipendenza al COVID a lungo termine fino al morbo di Alzheimer.
Oggi negli Stati Uniti, circa 1 adulto su 8 – ovvero circa 31 milioni di persone – dichiara di assumere un farmaco GLP-1. Secondo un sondaggio di KFF News del novembre 2025, circa 1 adulto su 5 ne ha fatto uso almeno una volta.
Tuttavia, la rapida diffusione di questi farmaci è stata accompagnata anche da un numero crescente di segnalazioni di effetti collaterali, tra cui problemi gastrointestinali, pancreatite acuta, maggiore incidenza di malattie della cistifellea e delle vie biliari, calcoli renali, artrite, disturbi del sonno, carie dentale, malnutrizione, perdita di capelli e perdita di densità ossea e massa muscolare.
Questi farmaci potrebbero anche essere collegati al cancro. La ricerca indica inoltre che potrebbero avere effetti collaterali di natura psicologica, tra cui l’apatia nei consumatori.
Secondo quanto riportato giovedì dal quotidiano The Independent, oltre 4.000 americani hanno intentato causa contro le case farmaceutiche, sostenendo che i farmaci abbiano causato effetti collaterali che hanno cambiato la loro vita e di cui le aziende non li avevano mai avvertiti.
Tra i querelanti figurano i familiari di persone decedute improvvisamente dopo aver assunto il farmaco. Altri querelanti affermano che il farmaco ha causato loro lo sviluppo di neuropatia ottica ischemica anteriore non arteritica (NAION), che provoca la perdita della vista.
Uno studio pubblicato la scorsa settimana sul British Journal of Ophthalmology ha rilevato che, tra le 1 persona su 10.000 che assumono farmaci e che soffrono di NAION, gli utilizzatori di Ozempic hanno una probabilità molto maggiore di sviluppare questa patologia rispetto agli utilizzatori di Wegovy.
Nel dicembre 2024, Novo ha dichiarato a The Defender di aver condotto un’indagine interna approfondita e di non aver riscontrato alcun collegamento tra la NAION e i suoi farmaci.
Nel giugno 2025, l’Agenzia europea per i medicinali ( EMA) ha confermato il collegamento tra i farmaci e la neuropatia ottica ischemica anteriore non arteritica (NAION). La condizione è riportata nell’etichetta europea, ma non compare ancora come effetto collaterale nell’etichetta statunitense di Ozempic. Quest’ultima si limita a raccomandare ai pazienti di contattare il proprio medico in caso di alterazioni della vista.
Brenda Baletti
Ph.D.
© 13 marzo 2026, Children’s Health Defense, Inc. Questo articolo è riprodotto e distribuito con il permesso di Children’s Health Defense, Inc. Vuoi saperne di più dalla Difesa della salute dei bambini? Iscriviti per ricevere gratuitamente notizie e aggiornamenti da Robert F. Kennedy, Jr. e la Difesa della salute dei bambini. La tua donazione ci aiuterà a supportare gli sforzi di CHD.
Renovatio 21 offre questa traduzione per dare una informazione a 360º. Ricordiamo che non tutto ciò che viene pubblicato sul sito di Renovatio 21 corrisponde alle nostre posizioni.
Iscriviti alla Newslettera di Renovatio 21
Immagine di pubblico dominio CCO via Flickr.
Alimentazione
Studio: le persone riprendono chili 4 volte più velocemente dopo aver smesso i farmaci per la perdita di peso
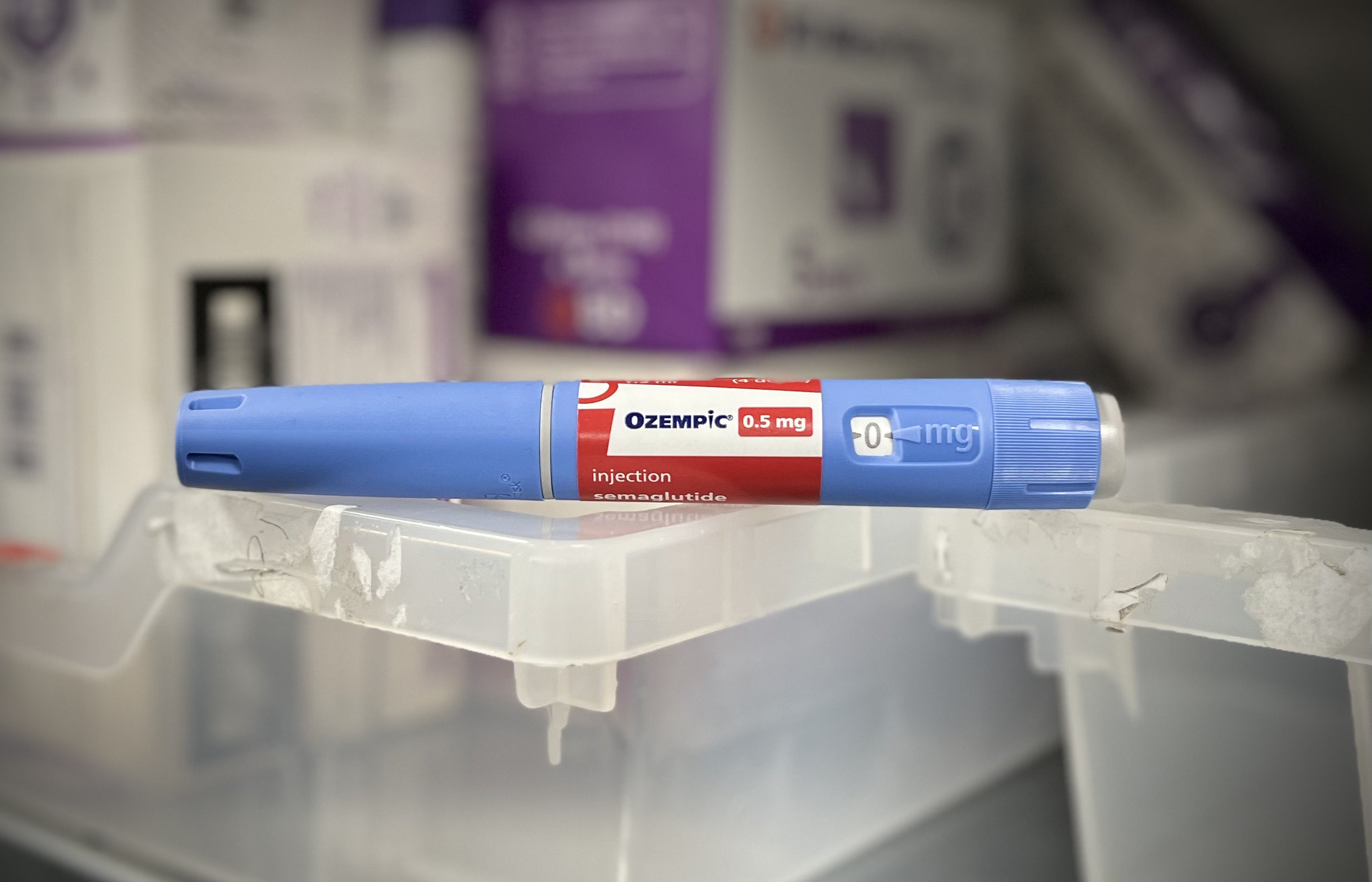
Aiuta Renovatio 21
Iscriviti alla Newslettera di Renovatio 21
Alimentazione
È arrivata la nuova era delle pillole dimagranti
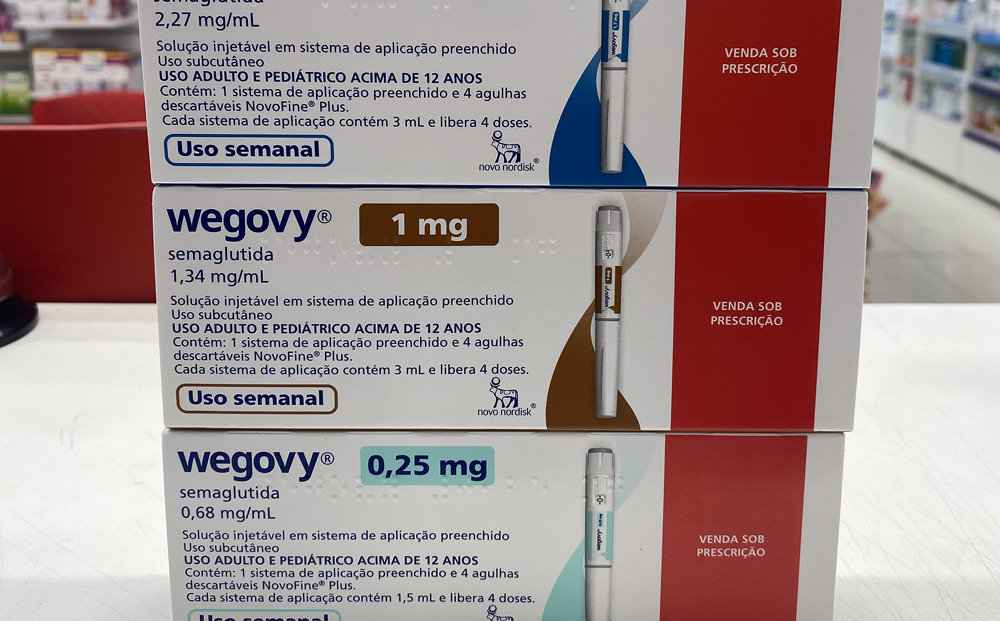
È iniziata una nuova fase per i farmaci dimagranti, dopo che la Food and Drug Administration (FDA) ha autorizzato la versione orale giornaliera del Wegovy prodotto da Novo Nordisk.
La nuova compressa, denominata da Novo «pillola Wegovy», impiega lo stesso principio attivo (semaglutide) presente nel Wegovy originale e in Ozempic, il farmaco gemello indicato per il trattamento del diabete.
Fino ad ora, Wegovy, Ozempic e i concorrenti di Eli Lilly come Zepbound e Mounjaro erano disponibili esclusivamente in forma iniettabile. Eli Lilly sta sviluppando la propria alternativa orale, nota come orforglipron. La pillola Wegovy ha dimostrato efficacia nella perdita di peso ed effetti collaterali analoghi alla versione iniettabile. Sarà commercializzata negli Stati Uniti a partire da gennaio.
In virtù di un accordo raggiunto con il presidente Trump, il prezzo di lancio della pillola Wegovy sarà di 149 dollari. «Riteniamo che ciò amplierà l’accesso e le opzioni per i pazienti», ha dichiarato in un’intervista alla CNN il dottor Jason Brett, responsabile medico statunitense di Novo Nordisk. «Sappiamo che ci sono alcuni pazienti che semplicemente non vogliono assumere un farmaco iniettabile».
Negli Stati Uniti, circa un adulto su otto fa uso di farmaci per dimagrire.
Sostieni Renovatio 21
Novo Nordisk sta sperimentando il semaglutide su bambini a partire dai sei anni di età e sono allo studio numerose nuove indicazioni per farmaci a base di semaglutide, tra cui trattamenti per le dipendenze, patologie neurologiche come l’Alzheimer e persino applicazioni anti-invecchiamento.
Nel 2023, i prodotti a base di semaglutide hanno generato a Novo Nordisk l’impressionante cifra di 21,1 miliardi di dollari, corrispondente a quasi due terzi del fatturato totale dell’azienda. Le vendite del farmaco nelle sue diverse formulazioni sono cresciute dell’89% rispetto all’anno precedente. Il 71% dei ricavi derivanti da questi farmaci proviene dal mercato statunitense.
Novo Nordisk è attualmente l’azienda più valutata d’Europa, con una capitalizzazione di mercato di 570 miliardi di dollari, superiore al PIL dell’intera Danimarca.
Negli ultimi mesi, l’enorme pubblicità e la diffusione di questi farmaci «miracolosi» hanno portato a una maggiore attenzione sugli effetti collaterali. Sono stati segnalati disturbi psichiatrici, squilibri ormonali (inclusa la riduzione del testosterone e la perdita della libido), inalazione del contenuto gastrico e persino casi di diarrea permanente.
Decine di migliaia di persone hanno intentato causa contro Novo Nordisk ed Eli Lilly per i danni fisici che affermano di aver subito. Per far fronte all’ondata di richieste di risarcimento potrebbero essere necessari esborsi ingenti, nell’ordine di centinaia di milioni o addirittura miliardi di dollari.
Come riportato da Renovatio 21, alcuni dati potrebbero indicare che i farmaci per la perdita di peso possono essere cancerogeni. A inizio anno l’Agenzia Europea per i Medicinali (EMA) aveva concluso che i farmaci a base di semaglutide, tra cui Ozempic, Wegovy e Rybelsus, aumentano il rischio di una grave patologia oculare che può portare alla perdita improvvisa della vista.
Iscriviti al canale Telegram ![]()
Come riportato da Renovatio 21, il rischio della cecità come effetto collaterale dell’Ozempic era stato segnalato in precedenza, andandosi ad aggiungere ad una lista crescente di effetti collaterali del farmaco.
Uno studio dell’anno scorso notava che le persone che assumono Ozempic e Wegovy hanno il 45% in più di probabilità di avere pensieri suicidi, una correlazione possibile emersa ancora due anni fa agli inizi della distribuzione del farmaco.
Nel 2023 la Food and Drug Administration (FDA), ente regolatore del farmaco negli Stati Uniti, aveva avvertito che l’Ozempic – approvato per il diabete ma usato off label per la perdita di peso – e Wegovy dovrebbero essere interrotti almeno due mesi prima della gravidanza, ma questi avvertimenti sono sepolti e i test a lungo termine non saranno completati per anni.
Iscriviti alla Newslettera di Renovatio 21
Immagine di Nelson R. de Lima Filho via Wikimedia pubblicata su licenza Creative Commons Attribution 4.0 International; immagine tagliata
-



 Vaccini2 settimane fa
Vaccini2 settimane faStudio su oltre un milione di bambini rileva la miocardite solo nei bambini vaccinati
-



 Pensiero2 settimane fa
Pensiero2 settimane faMao e il «blocco storico» che ha vinto il referendum
-


 Vaccini1 settimana fa
Vaccini1 settimana faProposte di legge USA per definire i vaccini a mRNA contro il COVID «armi di distruzione di massa»
-



 Pensiero5 giorni fa
Pensiero5 giorni faPizzaballa incontra il privilegio israeliano. Aspettando il Golem e l’Anticristo
-



 Spirito1 settimana fa
Spirito1 settimana faMons. Viganò, la Chiesa e l’intronizzazione dell’«arcivescova» anglicana: «Leone abbraccia l’eresia ecumenista»
-


 Economia1 settimana fa
Economia1 settimana faLa guerra in Iran e la rinazionalizzazione dell’industria italiana. Intervista al prof. Pagliaro
-



 Spirito2 settimane fa
Spirito2 settimane faMons. Viganò, cronologia del silenzio vaticano
-



 Salute1 settimana fa
Salute1 settimana faI malori della 13ª settimana 2026













