Big Pharma
CNN: la Bayer ha pagato milioni di medici per diffondere dispositivi per la contraccezione difettosi
A proposito di etica medica: questo articolo della CNN dello scorso luglio ci racconta della corruzione immonda della medicina operata da Big Pharma: e i medici, molti dei quali si ritrovano nella pagina Facebook di Renovatio 21 per difendere la categoria, ci sono stati alla grande, anche quando si tratta di infilare dentro il corpo delle loro pazienti dispositivi difettosi. Il futuro dell’umanità deve passare giocoforza attraverso la ristrutturazione dell’industria farmaceutica e la riformulazione totale della professione medica.
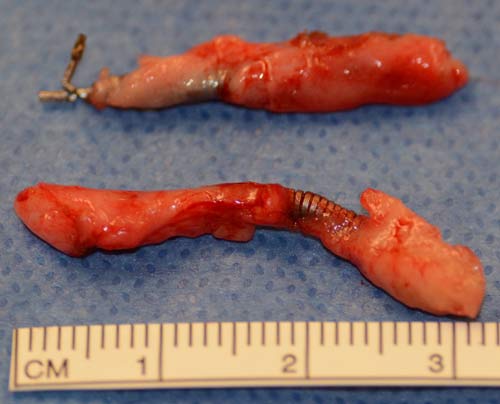
Quando Christina Potts stava cercando un contraccettivo permanente, il suo dottore era un entusiasta sostenitore di una e una sola opzione: Essure.
Secondo l’FDA, il dispositivo è associato a «gravi rischi tra cui dolore persistente, perforazione dell’utero e tube di Falloppio e migrazione delle bobine nel bacino o nell’addome»
Da agosto 2013 a dicembre 2017, la Bayer ha pagato 11.850 medici $ 2,5 milioni relativi a Essure per consulenze e servizi simili
Studi di scienziati presso l’ Università della Carolina del Nord , la Yale University , la George Washington University e la Harvard Medical School , tra gli altri, dimostrano che quando i medici sono pagati dalle compagnie farmaceutiche, sono più propensi a prescrivere farmaci fatti da quelle società.
Il documentario di Netflix presenta un gruppo di donne che hanno fatto pressioni sul Congresso per anni per far uscire Essure dal mercato. Il loro gruppo privato su Facebook, Essure Problems, conta oltre 37.000 membri, tra cui oltre 12.000 donne che affermano di aver subito un’isterectomia o un’altra procedura chirurgica per rimuovere il dispositivo, secondo la fondatrice del gruppo Angie Firmalino.
La Bayer dichiara che gli operatori sanitari «sono compensati per la loro esperienza e i servizi che forniscono all’industria farmaceutica, ed è appropriato ed etico per la Bayer compensare i professionisti medici per il tempo che dedicano a queste attività»
«Sembra una bustarella»
«Sembra una bustarella – dice il dottor Makary – sembra un falsare il sistema, sembra che l’azienda farmaceutica stia pagando i medici»
Dati su Essure
Secondo la FDA , gli eventi avversi segnalati «non possono essere interpretati o utilizzati isolatamente per trarre conclusioni sull’esistenza, la gravità o la frequenza dei problemi associati ai dispositivi» e «confermare se un dispositivo ha effettivamente causato un evento specifico può essere difficile basandosi unicamente sulle informazioni fornito in un determinato rapporto».
Big Pharma
La Bayer: gli europei dovranno pagare di più per i farmaci

Il colosso farmaceutico tedesco Bayer ha avvertito che le case farmaceutiche europee dovranno aumentare i prezzi dei nuovi farmaci in Europa per mantenere i profitti, a fronte delle pressioni statunitensi per ridurre i costi dei farmaci per i cittadini americani.
L’anno scorso, il presidente degli Stati Uniti Donald Trump ha emesso un ordine esecutivo per obbligare le grandi aziende farmaceutiche a confrontare i prezzi dei farmaci chiave venduti negli Stati Uniti con quelli di altri Paesi, citando differenze di prezzo ingiuste. A marzo, 16 importanti case farmaceutiche avevano raggiunto accordi con Washington per ridurre i prezzi sul mercato statunitense in cambio di tre anni di esenzione dai dazi.
Sebbene Bayer non fosse tra le aziende menzionate, il responsabile della sua divisione farmaceutica, Stefan Oelrich, ha dichiarato mercoledì a Bloomberg che l’azienda si sta preparando a un nuovo sistema di prezzi ed è in trattative con i governi di Europa, Giappone e altre nazioni ricche per spingere ad aumentare i prezzi dei nuovi farmaci al fine di compensare gli sconti offerti ai consumatori statunitensi.
«In Europa, dobbiamo aumentare il livello dei prezzi per il lancio di nuovi prodotti», ha dichiarato Oelrich a Bloomberg. «Altrimenti, come settore – e questo naturalmente vale anche per noi – ci troveremo ad affrontare ulteriori sconti negli Stati Uniti che non ci permetterebbero di recuperare le spese totali».
Aiuta Renovatio 21
Il dirigente della grande farmaceutica rilasciato dichiarazioni simili al Financial Times, avvertendo che gli europei dovranno pagare di più per i farmaci se la regione vuole rimanere un mercato attraente per i nuovi medicinali. In precedenza aveva già avvertito che collegare i prezzi statunitensi a quelli europei potrebbe costringere le aziende a scegliere tra i due mercati, poiché il lancio di un farmaco in Europa, dove i prezzi sono più bassi, rischia di compromettere i ricavi negli Stati Uniti.
Secondo quanto riportato mercoledì dall’agenzia Reuters, citando GlobalData, il numero di nuovi farmaci lanciati in Europa è diminuito di circa il 35% negli ultimi dieci mesi, a seguito dell’ordinanza di Trump. Alcune aziende hanno addirittura ritirato i propri prodotti dal mercato europeo. Amgen ha ritirato il farmaco per il colesterolo Repatha dalla Danimarca. Indivior ha ritirato i farmaci anti-dipendenza Subutex e Suboxone dalla Svezia e da altri mercati.
L’avvertimento di Oelrich giunge nel contesto di una più ampia frattura commerciale tra Stati Uniti e Unione Europea, iniziata con il ritorno di Trump alla Casa Bianca e culminata nell’accordo commerciale dello scorso anno, ampiamente considerato umiliante in Europa. L’accordo fissa al 15% il tetto massimo per le tariffe sulla maggior parte delle merci UE in ingresso negli Stati Uniti, mentre elimina le tariffe su alcune importazioni americane. Il blocco ha inoltre concordato di investire 600 miliardi di dollari negli Stati Uniti e di acquistare energia americana per un valore di 750 miliardi di dollari.
La Bayer è un’azienda che ha una lunga storia, con pieghe assai controverse come quella dell’eroina. Nel 1897, il chimico Felix Hoffmann della tedesca Bayer – la stessa azienda che pochi giorni prima aveva sintetizzato l’Aspirina – produsse la diacetilmorfina (eroina). La società la commercializzò dal 1898 con il nome «Heroin», derivato dal tedesco heroisch («eroico, potente»), come rimedio miracoloso: sedativo per la tosse, analgesico e, soprattutto, sostituto non assuefacente della morfina.
Bayer la promosse aggressivamente in tutto il mondo come farmaco da banco, persino per bambini e morfinomani. Nel 1899-1900 ne esportava in 23 Paesi e produceva circa una tonnellata all’anno. Le pubblicità la descrivevano come rimedio per tosse, dolori, tubercolosi e dipendenza da morfina. Centinaia di articoli scientifici (oltre 180 tra il 1899 e il 1905) ne esaltavano i benefici, ignorando o sottovalutando i rischi.
La realtà fu drammatica: l’eroina attraversa rapidamente la barriera emato-encefalica, si trasforma in morfina nel cervello e genera un’euforia più intensa, creando dipendenza più rapida e forte della morfina stessa. Ben presto medici e farmacisti osservarono tolleranza crescente, dosi sempre più alte e vera e propria assuefazione. Bayer smise di produrla commercialmente intorno al 1913, ma il danno era fatto: contribuì alla prima epidemia di oppioidi del Novecento.
Negli USA l’eroina divenne presto farmaco da ricetta (1914) e fu completamente bandita nel 1924 con l’Heroin Act. Nel frattempo aveva già creato migliaia di tossicodipendenti, inclusi ex morfinomani e pazienti trattati per banali raffreddori.
Iscriviti al canale Telegram ![]()
La vicenda dell’eroina rivela come l’entusiasmo per un nuovo «miracolo chimico», unito a insufficienti test di sicurezza e a un marketing spregiudicato, abbia trasformato una sostanza potenzialmente utile in una delle droghe più devastanti della storia, che ancora oggi miete vittime in tutte le società occidentali e non solo.
All’altezza della Seconda Guerra Mondiale, Bayer faceva parte del colosso chimico IG Farben. L’azienda utilizzò lavoro forzato nei campi di concentramento (soprattutto Auschwitz-Monowitz/Buna), dove morirono migliaia di prigionieri. Fornirono prodotti chimici e testarono farmaci su detenuti (inclusi esperimenti di Helmuth Vetter, medico Bayer e SS). IG Farben produsse anche lo Zyklon B usato nelle camere a gas. Dopo la guerra, alcuni dirigenti IG Farben (ex Bayer) furono processati a Norimberga; Bayer riassunse diversi ex nazisti condannati.
Negli anni Ottanta divisione Cutter Biological di Bayer produsse il Factor VIII per emofiliaci. Quando scoprirono la contaminazione da HIV, invece di distruggere le scorte (troppo costose), continuarono a vendere il prodotto non trattato termicamente in Asia, America Latina e altri Paesi in via di sviluppo per quasi un anno dopo aver lanciato la versione sicura in USA ed Europa. Risultato: migliaia di emofiliaci infettati da HIV e epatite C, molti morti. Bayer pagò centinaia di milioni di dollari in risarcimenti, senza tuttavia ammettere colpe.
Iscriviti alla Newslettera di Renovatio 21
Immagine di Atamari via Wikimedia pubblicata su licenza Creative Commons Attribution-Share Alike 3.0 Unported
Big Pharma
Bayer sfrutta i legami con la Washington di Trump per proteggere l’impero dei pesticidi

Sostieni Renovatio 21
La portata di Bayer nella cerchia ristretta di Trump
I legami più forti tra Bayer e l’amministrazione Trump coinvolgono un gruppo di lobbisti ed ex lobbisti della Florida che detengono il potere nella Washington di Trump: il capo dello staff Susie Wiles, il procuratore generale degli Stati Uniti Pam Bondi e Brian Ballard, che hanno impiegato sia Bondi che Wiles come lobbisti per anni prima che entrassero a far parte dell’amministrazione Trump. Wiles, una delle più influenti consigliere di Trump a Washington, ha lavorato per Ballard Partners come lobbista e poi come socia per un decennio, fino al 2022. Dal 2016 al 2022, ha anche lavorato come consulente senior per le campagne presidenziali di Trump. Ballard ha raccolto più di 50 milioni di dollari per la campagna di Trump del 2024 e ha fatto parte dei comitati finanziari per l’insediamento e la transizione del 2024; è ampiamente considerato una delle persone più influenti di Washington, DC, pur non ricoprendo un titolo governativo ufficiale. Lo studio di Ballard, Ballard Partners, è diventato lo studio di lobbying con i maggiori profitti a Washington nel 2025, stabilendo un record per l’ anno più redditizio per uno studio di lobbying nella storia degli Stati Uniti. L’azienda si è registrata per fare lobbying a favore di Bayer nel dicembre 2024. Ora l’azienda fa lobbying anche per l’American Chemistry Council (ACC), un’associazione di categoria che annovera Bayer tra i suoi membri aziendali. Sia Ballard che il suo socio, Daniel McFaul, che ha fatto parte del team di transizione presidenziale di Trump nel 2016-2017, sono registrati per fare lobbying sia per Bayer che per l’ACC. Secondo le dichiarazioni rilasciate dalle lobby federali, le due organizzazioni hanno versato a Ballard Partners una cifra complessiva di mezzo milione di dollari da quando Trump è stato eletto per la seconda volta. Una delle priorità dell’ACC quest’anno è la revisione del Toxics Substances Control Act, la principale legge nazionale sulle sostanze chimiche tossiche. Un nuovo disegno di legge repubblicano mira a restringere le prove scientifiche che le autorità di regolamentazione possono utilizzare per valutare i rischi per la salute e darebbe alle aziende chimiche un ruolo più ampio nella valutazione delle modalità di valutazione dei loro prodotti. In qualità di Procuratore Generale, Bondi guida il Dipartimento di Giustizia ed esercita un ampio potere sulla strategia legale federale e sulle posizioni del governo in tribunale. Come Wiles, Bondi si è alternata tra il suo incarico di lobbista presso Ballard Partners e ruoli a sostegno di Trump. Bondi è entrata a far parte di Ballard Partners nel gennaio 2019 per lanciare e presiedere la divisione corporate regulatory compliance dello studio. Ha lasciato lo studio più tardi nello stesso anno per assistere nella difesa legale di Trump per la sua prima inchiesta di impeachment, per poi tornare in Ballard Partners per cinque anni, dal 2020 al 2025, prima di assumere la carica di vertice del Dipartimento di Giustizia. Per altri dirigenti di Ballard Partners legati a Trump, consulta il nostro Bayer Lobby Tracker. Un altro legame tra Bayer e Wiles è la società di lobbying e pubbliche relazioni Mercury Public Affairs. Il capo dello staff di Trump è stato co-presidente di Mercury dal 2022 al novembre 2024, subito prima di entrare alla Casa Bianca. L’azienda si è registrata per fare lobbying a favore di Bayer nell’agosto 2025. Mentre era alla Mercury, Wiles è stato anche co-presidente della campagna presidenziale di Trump nel 2023 e nel 2024, secondo le dichiarazioni finanziarie. Tra i lobbisti registrati per Bayer presso Mercury Public Affairs c’è Bryan Lanza, che è stato vicedirettore delle comunicazioni per la campagna di Trump del 2016 e direttore delle comunicazioni per il primo team di transizione presidenziale di Trump. Lanza è entrato a far parte di Mercury nel 2017 ed è stato ospite frequente di programmi di informazione via cavo come sostituto e consigliere di Trump.Iscriviti al canale Telegram ![]()
Altri legami tra Bayer e la Casa Bianca
Un altro collaboratore chiave della Casa Bianca con legami con la rete legale di Bayer è Ryan Baasch, vice assistente di Trump al Presidente per la politica economica. In questo ruolo, Baasch contribuisce a tradurre l’agenda economica di Trump in una politica federale coordinata. Dal 2016 al 2021, Baasch è stato associato presso Latham & Watkins, uno studio legale che ha rappresentato Bayer nelle questioni relative all’accordo sul Roundup e Monsanto in un caso riguardante il dicamba. Lo studio ha inoltre rappresentato Monsanto e CropLife America in un caso di allerta sul glifosato. Un altro collaboratore vicino a Trump nel 2025, Trent Morse, è stato socio senior presso Ballard Partners dal 2020 al 2022, per poi passare a Mercury Public Affairs come vicepresidente senior. In qualità di vice assistente del presidente e vicedirettore del personale presidenziale per otto mesi, Morse ha fatto parte del team responsabile del reclutamento, della selezione e della raccomandazione dei candidati per le nomine politiche in tutto il ramo esecutivo. Ha lasciato la Casa Bianca ad agosto per un incarico di lobbying.I legami dei funzionari dell’USDA con la Bayer
L’USDA supervisiona le politiche agricole, i sistemi colturali e le approvazioni delle biotecnologie, definendo i sussidi, la ricerca e le decisioni sulle piantagioni che guidano la domanda di sementi e prodotti chimici Bayer. L’ agenzia è da tempo criticata per il suo servilismo nei confronti dell’industria chimica, e l’amministrazione Trump non fa eccezione. Tra gli attuali funzionari dell’USDA che hanno legami con Bayer e i suoi alleati dell’industria chimica figurano:- Stephen Vaden, vicesegretario all’agricoltura, è un ex collaboratore di Jones Day (2014-2017), uno studio legale che ha rappresentato Bayer nell’acquisizione di Monsanto, e di Squire Patton Boggs (2011-2014), che ha rappresentato Bayer e Monsanto in casi riguardanti glifosato e PCB.
- Richard Fordyce, sottosegretario alla produzione agricola e alla conservazione, è l’ex direttore per la crescita del business agricolo dell’agenzia di pubbliche relazioni e marketing Osborn Barr Paramore (2021-2025), che per anni è stata l’agenzia di pubbliche relazioni di Bayer. Ex direttore dello United Soybean Board, Fordyce è stato amministratore della Farm Service Agency durante il primo mandato di Trump.
- Scott Hutchins, sottosegretario per la ricerca, l’istruzione, l’economia e responsabile scientifico, ha trascorso oltre 30 anni presso Dow AgroSciences (ora Corteva), ricoprendo di recente il ruolo di direttore globale di Ricerca e Sviluppo. Ha ricoperto lo stesso ruolo presso l’USDA durante la prima amministrazione Trump.
- Pat Swanson, amministratrice della Risk Management Agency, è stata direttrice dei gruppi di pressione American Soybean Association e Iowa Soybean Association, dove si è battuta per i pesticidi della Bayer.
- Bill Beam, amministratore della Farm Service Agency, ha prestato servizio per nove anni nello United Soybean Board, che collabora con Bayer su iniziative di ricerca. In precedenza, Beam ha ricoperto il ruolo di vice amministratore per i programmi agricoli presso la FSA (2018-2021).
La ricerca della prelazione federale da parte di Bayer
Il caso Bayer davanti alla Corte Suprema ha una posta in gioco elevata per la tutela della salute pubblica e per il diritto legale dei cittadini di chiamare le aziende a rispondere delle proprie azioni in tribunale. La prelazione federale, ovvero l’idea che la legge federale possa prevalere sulla legge statale in alcune circostanze, è da tempo una priorità per le aziende chimiche e alimentari che desiderano un unico standard nazionale, spesso più debole, per la regolamentazione e la responsabilità, mentre i gruppi di consumatori e di tutela della salute sostengono che gli stati debbano mantenere il diritto di stabilire standard più elevati in materia di salute e sicurezza. La questione è centrale nel caso Bayer davanti alla Corte Suprema: l’azienda sostiene che, poiché l’EPA ha approvato il glifosato, le richieste di risarcimento per cancro legate al Roundup dovrebbero essere escluse dalle leggi statali sulla mancata allerta. La posizione del governo federale sulla prevalenza delle approvazioni dei pesticidi sulle leggi statali è cambiata da un’amministrazione all’altra, sottolineando quanto l’esito dipenda da chi detiene il potere e da chi lo influenza. Nel maggio 2025, due avvocati d’appello con una consolidata esperienza presso il Dipartimento di Giustizia, Jennifer Scheller Neumann e Amelia Yowell, si sono unite a Holland & Hart LLP, uno studio legale che fornisce servizi legali e di lobbying. Un mese prima, lo studio si era registrato per svolgere attività di lobbying per conto di Bayer. Neumann ha trascorso 20 anni presso la Divisione Ambiente e Risorse Naturali del Dipartimento di Giustizia, ricoprendo di recente il ruolo di capo della sezione d’appello, supervisionando tutti i contenziosi d’appello riguardanti le leggi federali in materia ambientale. È stata firmataria della memoria amicus curiae del Dipartimento di Giustizia del 2019 presso la Corte d’Appello del 9° Circuito a sostegno di Monsanto (ora Bayer). La memoria sostiene che l’approvazione del glifosato da parte dell’EPA prevale sulle leggi statali in materia di mancata allerta. L’amministrazione Biden ha ribaltato tale posizione nel 2022, esortando la Corte Suprema a respingere il caso Bayer sulla base del presupposto che la legge federale sui pesticidi non dovesse prevalere sulle leggi statali in materia di mancata allerta. Il Dipartimento di Giustizia di Trump ha ribaltato nuovamente la posizione nel 2025, sostenendo che la posizione dell’era Biden era errata e che le giurie non avrebbero dovuto mettere in discussione la scienza dell’EPA. Le argomentazioni orali davanti alla Corte Suprema sono previste per il 27 aprile. Una vittoria della Bayer potrebbe trasformare le approvazioni dei pesticidi da parte dell’EPA in uno scudo di responsabilità a livello nazionale, elevando il lento e spesso dominato processo di valutazione chimica dell’agenzia a una parola definitiva sulla sicurezza dei pesticidi, in un momento in cui continuano a emergere ricerche sottoposte a revisione paritaria che collegano l’esposizione ai pesticidi al cancro, ai danni neurologici e ad altre malattie croniche. Come ha avvertito Nathan Donley del Center for Biological Diversity, un simile precedente significherebbe che «l’unica cosa che conta legalmente nel determinare la sicurezza di un pesticida è ciò che l’EPA afferma essere vero, anche se tali affermazioni ignorano completamente la migliore scienza disponibile».Sostieni Renovatio 21
Riduzione della capacità dell’EPA
Gli alleati della Bayer sono presenti anche all’interno dell’agenzia statunitense incaricata della tutela della salute e dell’ambiente, in posizioni in cui influenzano quali sostanze chimiche e pesticidi vengono approvati e come questi prodotti vengono regolamentati. I lobbisti dell’industria chimica ora occupano i primi quattro posti presso l’Office of Chemical Safety and Pollution Prevention (OCSPP) dell’EPA, la divisione responsabile della regolamentazione di sostanze chimiche e pesticidi. I funzionari dell’EPA hanno allentato gli standard etici per consentirlo. Douglas Troutman, assistente amministrativo presso l’OCSPP, è l’ex co-CEO e capo lobbista dell’American Cleaning Institute, che rappresenta i principali produttori di prodotti chimici. Troutman ha lavorato presso il gruppo di pressione per 17 anni prima di entrare nell’amministrazione Trump. Nancy Beck, vicedirettore assistente principale dell’OCSPP, è stata direttrice senior dell’ACC, un gruppo di pressione che rappresenta Bayer, Dow Chemical, DuPont e altri produttori chimici, dal 2012 al 2017. Durante la prima amministrazione Trump, ha ricoperto ruoli consultivi alla Casa Bianca presso il Consiglio Economico Nazionale e l’Ufficio di Gestione e Bilancio. Tra le amministrazioni Trump, ha lavorato presso Hunton Andrews Kurth, uno studio legale che offre, tra gli altri servizi, la difesa legale in contenziosi sul glifosato alle aziende che affrontano cause legali per richieste di risarcimento per cancro. Lynn Ann Dekleva, vicedirettrice associata dell’OCSPP per i nuovi prodotti chimici, ha ricoperto questo ruolo anche durante la prima amministrazione Trump. Nel frattempo, è stata direttrice senior presso il gruppo di pressione ACC. È una veterana trentennale dell’azienda chimica DuPont, dove ha lavorato come responsabile di programma e ingegnere. Kyle Kunkler, vicedirettore aggiunto dell’OCSPP per i pesticidi, è un ex lobbista dell’industria dei pesticidi. È stato direttore degli affari governativi, con particolare attenzione a biotecnologie e pesticidi, per l’American Soybean Association dal 2020 al 2025, e in precedenza ha trascorso tre anni gestendo gli affari governativi in materia di alimentazione e agricoltura per il gruppo di pressione della Biotechnology Innovation Organization. CropLife America, il principale gruppo di pressione dell’industria dei pesticidi, gli ha conferito il premio «Rising Star» nel 2020. Altri funzionari dell’EPA legati alla Bayer includono:- Steven Cook, vicedirettore aggiunto dell’Office of Land and Emergency Management (OGE), supervisiona i siti Superfund. Bayer è associata a diversi siti Superfund per la sua produzione di pesticidi e prodotti chimici. Cook ha trascorso oltre 20 anni come consulente legale interno per LyondellBasell, una delle più grandi aziende al mondo nel settore delle materie plastiche e dei prodotti chimici. LyondellBasell ha una joint venture al 50% con Bayer (un impianto di produzione di ossido di propilene e stirene monomero). L’amministratore delegato di LyondellBasell, Peter Vanacker, è presidente del consiglio di amministrazione dell’ACC.
- Aaron Szabo, amministratore assistente per l’aria e le radiazioni (nominato nel luglio 2025), è stato socio e lobbista presso il CGCN Group (2018-2023), che è stato registrato per fare lobbying per l’ACC negli ultimi dieci anni. Dal 2023 al 2024, è stato direttore senior e avvocato presso Faegre Drinker Biddle & Reath, dove ha rappresentato interessi chimici, tra cui l’ACC, prima di tornare all’EPA nel gennaio 2025.
- Alex Dominguez, vice amministratore aggiunto per le fonti mobili, era un lobbista registrato presso Massie Partners, dove rappresentava la National Corn Growers Association, un’associazione i cui membri sono consumatori di sementi e pesticidi Bayer. Ha ricoperto tale ruolo dal 2023 a gennaio 2025.
Aiuta Renovatio 21
Altri funzionari di Trump legati alla Bayer
In qualità di assistente segretario alla legislazione presso il Dipartimento della Salute e dei Servizi Umani degli Stati Uniti (HHS), Gary Andres è un importante collegamento tra l’HHS e il Congresso. In precedenza, è stato vicepresidente esecutivo senior per gli affari pubblici presso la Biotechnology Innovation Organization, il principale gruppo di categoria per le aziende biotecnologiche, tra cui Bayer. Presso BIO, Andres ha diretto la strategia di lobbying per l’intero settore biotecnologico, inclusa la difesa del quadro normativo per gli OGM e i prodotti agrochimici associati. In precedenza, ha lavorato presso la società di lobbying Dutko Worldwide, che ha rappresentato Bayer. Anche il Segretario dei trasporti statunitense Sean Duffy ha legami con una società di lobbying della Bayer; è stato consulente senior e membro del comitato consultivo del BGR Group dal 2019 al 2023 ed è stato un lobbista registrato per la società nel 2020, sebbene non vi sia alcuna traccia che abbia fatto lobbying per la Bayer.13 società di lobbying che lavorano per Bayer a Washington
La spesa diretta di Bayer per attività di lobbying è significativa, ma la sua influenza politica si espande considerevolmente se considerata insieme ai gruppi commerciali e delle materie prime alleati che insieme formano una rete di lobbying ben finanziata e coordinata. Nel 2025, Bayer ha assunto almeno 13 società di lobbying e almeno 49 lobbisti registrati per fare lobbying per l’azienda (inclusi i sei lobbisti interni di Bayer) a partire dal quarto trimestre, come mostrano le dichiarazioni federali. Lo scorso anno, Bayer ha speso almeno 9,19 milioni di dollari in attività di lobbying a livello federale. Pur non rientrando tra le singole aziende con la spesa più elevata in attività di lobbying a Washington, il settore agroalimentare si è classificato al nono posto con 219,9 milioni di dollari di spese di lobbying nel 2025, l’anno più alto mai registrato per il settore. Includiamo il totale del settore perché l’influenza di Bayer è amplificata da un sistema agroalimentare industriale integrato che agisce di concerto, dalle colture di materie prime dipendenti dai pesticidi agli allevamenti intensivi e alla produzione di alimenti ultra-processati, per plasmare le politiche a suo favore. All’interno del settore, tra i gruppi che esercitano direttamente pressioni per politiche favorevoli sui pesticidi figurano associazioni commerciali che rappresentano i produttori di pesticidi (ACC e CropLife America) e gruppi di prodotti di base come la National Corn Growers Association e l’American Soybean Association, che si affidano ai prodotti Bayer. Nel 2025, questi quattro gruppi hanno speso complessivamente 22 milioni di dollari in attività di lobbying a livello federale, con la registrazione di altri 23 lobbisti nel quarto trimestre. L’attività di lobbying della Bayer dello scorso anno (fonte: OpenSecrets) ha raggiunto il livello più alto degli ultimi anni, ma è stata inferiore al picco raggiunto dall’azienda nel 2016, 2017 e 2018, appena prima della fusione Bayer/Monsanto e in seguito alla scoperta del 2015 da parte dell’agenzia per il cancro dell’Organizzazione mondiale della sanità che il glifosato è un probabile cancerogeno per l’uomo. Questi numeri non riflettono il quadro completo delle attività di lobbying di Bayer. Il Lobbying Disclosure Act richiede la registrazione solo dopo aver raggiunto determinate soglie di spesa e attività, quindi i documenti pubblici non coprono tutte le attività di influenza retribuita svolte a Washington. Inoltre, non riflettono l’attività a livello statale. La spesa per i PAC (Committee for Governance) relativa ai pesticidi è aumentata vertiginosamente alla fine del 2024, poiché le aziende hanno cercato di limitare i risarcimenti danni nei tribunali di tutto il paese. Solo in Iowa, Bayer ha speso una cifra record l’anno scorso nel tentativo di approvare un disegno di legge sull’immunità statale che i critici hanno definito «Cancer Gag Act» [legge bavaglio sul cancro, ndt]. Per saperne di più sulla forza di lobbying della Bayer, consulta il nostro Bayer Lobby Tracker.Iscriviti alla Newslettera di Renovatio 21
Altri lobbisti legati a Trump
Gli scienziati politici hanno documentato da tempo come il lobbying influenzi le politiche pubbliche, garantendo l’accesso ai decisori e aiutando le aziende a trasformare le loro priorità in leggi e regolamenti. Queste dinamiche aiutano a spiegare come aziende come Bayer possano tradurre l’accesso a Washington in concreti successi politici. La nostra analisi mostra che oltre 30 persone che ricoprono posizioni di leadership presso società di lobbying gestite da Bayer hanno legami diretti con l’attuale o precedente amministrazione di Trump o con le campagne presidenziali. Molti di questi lobbisti non sono registrati personalmente per fare lobbying per Bayer, ma potrebbero fornire assistenza in modi che non comportano la registrazione, ad esempio fornendo consulenza ai lobbisti Bayer dell’azienda. Come già accennato in precedenza, Ballard Partners, lo studio legale presso cui lavoravano sia Wiles che Bondi e gestito da uno dei maggiori finanziatori politici di Trump, rappresenta un collegamento fondamentale tra Bayer e l’orbita di Trump. Oltre a Brian Ballard e Daniel McFaul, i due lobbisti dello studio registrati per fare lobbying sia per Bayer che per l’ACC, altri soci di Ballard hanno legami con Trump: Hunter Morgen, partner dello studio con sede a Washington, ha ricoperto per oltre tre anni posizioni di rilievo durante la prima amministrazione Trump, come assistente speciale del presidente e consulente senior per le politiche e la strategia alla Casa Bianca, lavorando su questioni commerciali e di immigrazione con Peter Navarro e Stephen Miller. Prima del suo incarico alla Casa Bianca, Morgen è stato consulente politico per il Dipartimento di Stato presso l’Ufficio per le politiche e la pianificazione. In precedenza, aveva lavorato nel team di transizione e campagna presidenziale di Trump del 2016. Nel 2020, Trump ha nominato Morgen nel Consiglio Presidenziale per il Miglioramento dell’Architettura Civile Federale. Morgen, insieme a Brian Ballard, Daniel McFaul, Syl Lukas (socio senior di Ballard) e Wiles, è stato incluso nell’elenco dei donatori invitati a un gala nell’ottobre 2025 per la nuova sala da ballo dell’ala est di Trump, del valore di 250 milioni di dollari. Mike Rubino, un altro partner di Ballard a Washington, è stato tra i primi ad essere assunto da Trump durante la campagna presidenziale del 2016, dove ha ricoperto il ruolo di consulente senior, dirigendo le operazioni in 10 stati e vincendone nove, secondo la sua biografia. Entrò a far parte della prima amministrazione Trump come alto funzionario presso l’HHS prima di passare al settore privato, dove lavorò al fianco di Corey Lewandowski, attualmente una figura chiave presso il dipartimento della Sicurezza Interna degli Stati Uniti. William Russell, socio di Ballard DC, è stato l’assistente responsabile dei viaggi quotidiani e della logistica di Trump per quasi quattro anni durante la prima amministrazione. Russell ha lavorato anche alle campagne elettorali di Trump del 2016 e del 2024. Brian Hughes, socio di Mercury Public Affairs, l’altra società di lobbying presso cui Wiles aveva precedentemente lavorato, è stato capo dello staff della NASA da maggio a dicembre 2025. È entrato a far parte di Mercury nel gennaio 2026. Hughes è stato responsabile della campagna elettorale di Trump in Florida nel 2024 e direttore delle comunicazioni per il team di transizione di Trump. Danielle Alvarez, un’altra partner di Mercury, ha ricoperto ruoli di comunicazione e consulenza nelle campagne elettorali di Trump del 2020 e del 2024. Altri legami tra la lobby della Bayer e la Casa Bianca di Trump includono:- Amy Swonger, dirigente di Invariant, un’azienda registrata per fare lobbying a favore di Bayer, ha lavorato nell’ufficio esecutivo del presidente per gran parte del primo mandato di Trump, come assistente del presidente e come direttrice e vicedirettrice degli affari legislativi.
- Jordan Bonfitto, direttore di Invariant, è stato consulente politico presso il Consiglio Economico Nazionale nella prima Casa Bianca di Trump, concentrandosi sui portafogli agricolo e biotecnologico. Da febbraio a ottobre 2025, Bonfitto è stato capo dello staff per i programmi di marketing e regolamentazione presso l’USDA sotto la Segretaria Brooke Rollins. È entrato a far parte di Invariant a novembre.
Iscriviti alla Newslettera di Renovatio 21
Big Pharma
Bayer punta sulla cura del Parkinson dopo decenni di vendita di prodotti come il glifosato legati alla malattia

Renovatio 21 traduce questo articolo per gentile concessione di Children’s Health Defense. Le opinioni degli articoli pubblicati non coincidono necessariamente con quelle di Renovatio 21.
Bayer sta avviando una sperimentazione clinica di Fase 3 per un trattamento del Parkinson a base di cellule staminali attraverso la sua controllata BlueRock, nonostante l’azienda stia affrontando migliaia di cause legali relative ai pesticidi collegati alla malattia. Questa mossa evidenzia il duplice ruolo di Bayer nel contribuire al Parkinson e nel cercare di trarne profitto.
Bayer sta lanciando un nuovo trattamento sperimentale per il morbo di Parkinson, nonostante il colosso farmaceutico e chimico continui a trarre profitto dalla vendita di pesticidi collegati alla malattia.
La società ha annunciato la scorsa settimana che la sua sussidiaria BlueRock Therapeutics LP ha avviato una sperimentazione clinica di fase 3 per il bemdaneprocel, un farmaco progettato per sostituire le cellule cerebrali produttrici di dopamina uccise dalla malattia neurodegenerativa.
Il farmaco deriva da cellule staminali impiantate chirurgicamente nel cervello di una persona affetta dal morbo di Parkinson. Una volta impiantate, le cellule staminali possono svilupparsi in neuroni dopaminergici maturi, contribuendo a riformare le reti neurali colpite dal Parkinson.
Ripristinano «potenzialmente» la funzionalità motoria e non motoria dei pazienti. Il farmaco è stato approvato dalla Food and Drug Administration statunitense nel 2021.
Bemdaneprocel sarà probabilmente disponibile sul mercato tra anni, eppure Bayer sta investendo molto nelle infrastrutture produttive per i futuri prodotti di terapia cellulare e genica. Parte di questo sforzo include la costruzione di uno stabilimento da 250 milioni di dollari in California, secondo Reuters.
Le tecnologie di terapia cellulare e genica contro il cancro stanno già generando profitti per altre aziende, ma BlueRock è la prima azienda a portare una terapia cellulare per il Parkinson alla fase 3 degli studi clinici.
Le difficoltà finanziarie della Bayer derivano in parte dai brevetti scaduti su due dei suoi farmaci di successo: l’anticoagulante Xarelto e il medicinale per gli occhi Eylea.
Ma i maggiori problemi finanziari di Bayer sono radicati nell’acquisizione di Monsanto nel 2018, secondo Reuters. Il glifosato, un diserbante di Monsanto, è collegato al cancro e al Parkinson, le stesse malattie da cui Bayer potrebbe trarre profitto con un nuovo trattamento.
Finora, Bayer ha pagato circa 11 miliardi di dollari per risolvere le cause legali relative al glifosato e si stima che siano ancora pendenti 67.000 cause legali nei suoi confronti.
Iscriviti al canale Telegram ![]()
Molti dei pesticidi della Bayer sono collegati al Parkinson
Il morbo di Parkinson è il disturbo neurologico in più rapida crescita al mondo, caratterizzato dalla perdita di neuroni nella parte del cervello che produce dopamina e che è responsabile del controllo motorio.
Sebbene non esista una cura nota per il Parkinson, esistono alcune cause note. Studi dimostrano che l’esposizione a diversi pesticidi è fortemente correlata allo sviluppo della malattia.
I collegamenti più ampiamente segnalati tra pesticidi e morbo di Parkinson riguardano l’erbicida paraquat della Syngenta.
Attraverso un’indagine sui documenti interni di Syngenta, il giornalista Carey Gillam ha rivelato che l’azienda era consapevole che il suo pesticida causava cambiamenti neurologici che sono il segno distintivo della malattia, ma lavorava segretamente per insabbiare le prove scientifiche del collegamento.
Tuttavia, studi recenti collegano anche l’esposizione ad altri pesticidi alla malattia.
Numerosi studi di casi, uno studio epidemiologico, studi sugli animali e recenti studi che esaminano molteplici esposizioni a pesticidi dimostrano che il glifosato, una nota neurotossina, probabilmente gioca un ruolo nel Parkinson.
Tuttavia, gli scienziati che scrivono sulle più importanti riviste mediche affermano che sono necessarie ulteriori ricerche e una migliore regolamentazione, citando il legame poco studiato tra glifosato e Parkinson come esempio paradigmatico del problema.
Parte del problema, affermano, è che sono le aziende produttrici di pesticidi a condurre la maggior parte delle ricerche, e la maggior parte di queste riguarda singoli pesticidi in modo isolato.
Nuove prove dimostrano che il Parkinson è anche – e forse più frequentemente – collegato all’esposizione a «cocktail» di pesticidi. Questi causano «una neurotossicità maggiore per i neuroni dopaminergici rispetto a qualsiasi singolo pesticida», perché i diversi pesticidi hanno meccanismi d’azione diversi. Se combinati, possono causare danni neurologici maggiori.
Una ricerca pubblicata su Nature Communications ha esaminato la storia dell’esposizione chimica dei pazienti affetti da Parkinson e ha identificato 53 pesticidi implicati nella malattia.
Tra le 10 sostanze chimiche identificate come direttamente tossiche per i neuroni collegate al Parkinson figurano pesticidi, erbicidi e fungicidi prodotti dalla Bayer.
Tra questi ci sono l’endosulfan, prodotto dall’azienda ma gradualmente eliminato in risposta alle pressioni internazionali; il diquat, un ingrediente chiave utilizzato dalla Bayer per sostituire il glifosato nel Roundup e vietato nell’UE, nel Regno Unito e in Cina; e i fungicidi contenenti solfato di rame e folpet.
Un altro studio ha identificato l’esposizione a lungo termine a 14 pesticidi con un aumento del rischio di morbo di Parkinson nelle persone che vivono nella regione delle Montagne Rocciose e delle Grandi Pianure.
I tre pesticidi con l’effetto più forte sono stati simazina, atrazina e lindano. Bayer produce diversi pesticidi contenenti simazina e atrazina. Bayer in precedenza utilizzava il lindano nei suoi prodotti, ma ne ha gradualmente eliminato l’uso come pesticida agricolo negli Stati Uniti.
Bayer è una delle quattro aziende, insieme a Syngenta, Corteva e BASF, che controllano da anni il mercato mondiale dei pesticidi.
Negli Stati Uniti, l’azienda ha tentato di proteggersi da ulteriori contenziosi sui rischi per la salute causati dai suoi prodotti chimici, sostenendo una legislazione a livello federale e statale che renderebbe più difficile per gli stati regolamentare i pesticidi o per le persone danneggiate dai prodotti agrochimici fare causa ai produttori.
Brenda Baletti
Ph.D.
© 1 ottobre 2025, Children’s Health Defense, Inc. Questo articolo è riprodotto e distribuito con il permesso di Children’s Health Defense, Inc. Vuoi saperne di più dalla Difesa della salute dei bambini? Iscriviti per ricevere gratuitamente notizie e aggiornamenti da Robert F. Kennedy, Jr. e la Difesa della salute dei bambini. La tua donazione ci aiuterà a supportare gli sforzi di CHD.
Renovatio 21 offre questa traduzione per dare una informazione a 360º. Ricordiamo che non tutto ciò che viene pubblicato sul sito di Renovatio 21 corrisponde alle nostre posizioni.
Iscriviti alla Newslettera di Renovatio 21
Immagine di Mister F. via Flickr pubblicata su licenza CC BY-NC-SA 2.0
-



 Pensiero1 settimana fa
Pensiero1 settimana faLa scomunica dei bambini
-



 Pensiero2 settimane fa
Pensiero2 settimane faDifesa di Nicole Minetti
-



 Gender2 settimane fa
Gender2 settimane faRapporto del Sinodo suggerisce che le relazioni omosessuali non sono peccato
-



 Intelligenza Artificiale2 settimane fa
Intelligenza Artificiale2 settimane faAvere paura dell’IA. E dello Stato moderno
-



 Gender2 settimane fa
Gender2 settimane faMons. Strickland: il rapporto del Sinodo sull’omosessualità è un «attacco diretto» all’insegnamento cattolico
-



 Salute1 settimana fa
Salute1 settimana faI malori della 19ª settimana 2026
-



 Misteri2 settimane fa
Misteri2 settimane faPastori protestanti americani informati di preparare le congregazioni alle rivelazioni sugli UFO
-



 Misteri1 settimana fa
Misteri1 settimana faIl Pentagono desecrata i documenti sugli UFO: ecco i video
















