Big Pharma
Quando la cura è la causa: il caso della lingua pelosa verde
Negli anni 60 in Giappone una strana epidemia avrebbe dovuto far scattare l’allarme in tutto il mondo, poiché molto spesso sono proprio le terapie mediche a peggiorare la situazione.
Per Keiko Yamaguchi tutto cominciò con la diarrea. Qualche settimana più tardi sopraggiunse un torpore alle dita dei piedi. Erano i primi mesi del 1967. Un anno più tardi, alla fine del 1968, la giovane ventiduenne Keiko si ritrovò cieca e paralizzata dalla vita in giù.
Si stima che almeno 900 persone persero la vita a causa di questa patologia
In Giappone soltanto, più di 11.000 persone (tra cui Keiko ) furono vittime di una misteriosa epidemia esplosa tra il 1955 e il 1970. Alcuni casi furono denunciati anche in altri Paesi, tra cui Gran Bretagna, Svezia, Messico, India, Australia. Tuttavia l’epidemia colpì soprattutto il Giappone, dove si stima che almeno 900 persone persero la vita a causa di questa patologia che i medici successivamente identificheranno con il nome neuropatia mielo-ottica subacuta (in inglese subacute myelo-optic neuropathy da cui l’acronimo SMON) dove la parola “mielo” deriva dalla parola greca che identifica il midollo spinale, la parola “ottica” fa riferimento alla vista e la parola neuropatia indica una patologia che colpisce i nervi.
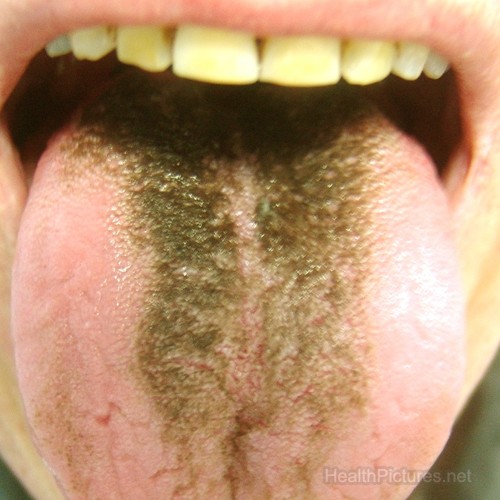
Un numero ancora incerto di pazienti invece vide la propria lingua diventare verde e pelosa
Generalmente la malattia inizia con attacchi di vomito e diarrea e con l’avanzare di questa, alcuni pazienti vengono colpiti da cecità e paralisi, proprio come Keiko. Un numero ancora incerto di pazienti invece vide la propria lingua diventare verde e pelosa: sulla lingua, infatti, spuntarono dei peletti verdi (o perlomeno qualcosa che vi somigliava). Per altri il colore verde si manifestò nelle urine.
La patologia non risparmiò nemmeno i membri della famiglia e contagiò anche medici e infermieri che cercarono di curarla. Una stima approssimativa stabilisce che la morte sopraggiunse per una percentuale di pazienti che va dal 5 al 10%.
La morte sopraggiunse per una percentuale di pazienti che va dal 5 al 10%
Che cosa causò l’epidemia? Negli anni ‘60 fu proprio il Giappone, il Paese più colpito, a promuovere numerosi programmi di ricerca per scoprirlo. I dottori pensarono di avere la risposta in pugno quando i ricercatori che stavano studiando i malati di SMON isolarono l’echovirus, conosciuto per essere la causa di problemi intestinali.
Presto però nei pazienti vennero rintracciati altri virus, inclusi il virus Coxakie e l’herpesvirus. La scoperta di quest’ultimo creò un certo entusiasmo, poiché è risaputo che l’herpesvirus colpisce il sistema nervoso. A una a una però tutte queste scoperte furono smentite poiché i ricercatori indipendenti non riuscirono a replicare le scoperte precedenti fatte in laboratorio.
Numerose furono le cause considerate e poi escluse. Nessun agente patogeno dell’acqua potabile fu mai rintracciato. E i pesticidi? Anche questa ipotesi fu scartata quando uno studio rivelò che gli agricoltori affetti da SMON erano meno dei non agricoltori, pur essendo i soggetti a questi maggiormente esposti.
Un farmacologo fece una scoperta rivelatrice: quanto pare la malattia derivava dall’assunzione farmaco: il cliochinolo, un medicinale utilizzato per la cura della dissenteria amebica
L’euforia tornò quando i ricercatori scoprirono che molte vittime avevano assunto due tipologie diverse di antibiotici, anche se sembrava improbabile che due diversi antibiotici potessero entrambi improvvisamente essere la causa della stessa malattia rara. Tuttavia, come notano gli esperti, i pazienti avevano assunto l’antibiotico solo dopo aver manifestato i primi sintomi della SMON.
Più tardi, alla fine del 1970 e tre anni dal respingimento della teoria degli antibiotici, un farmacologo fece una scoperta rivelatrice. A quanto pare i due presunti diversi antibiotici non erano altro che due brand diversi dello stesso farmaco: il cliochinolo, un medicinale utilizzato per la cura della dissenteria amebica o amebiasi. Inoltre fu svelato che la lingua verde pelosa e l’urina verde erano causate dalla dissoluzione del cliochinolo nel corpo dei pazienti. A un mese dalla rivelazione, il cliochinolo venne bandito in Giappone e l’epidemia di SMON, uno dei maggiori disastri farmaceutici della storia, conobbe un’improvvisa battuta d’arresto.
L’epidemia di SMON, uno dei maggiori disastri farmaceutici della storia
Sembra che l’epidemia colpì in particolar modo il Giappone in parte perché il farmaco veniva utilizzato di routine per curare non solo la dissenteria, ma anche per prevenire la diarrea del viaggiatore e varie forme di disturbi addominali. E anche perché i medici giapponesi erano soliti prescrivere il farmaco con dosi più elevate e per periodi di assunzione più lunghi di quanto non fosse abitualmente fatto negli altri Paesi.
Altra idea abbastanza convincente era l’illusione che la SMON fosse contagiosa. Infatti, famigliari, dottori e infermieri, pensando di proteggersi, assumevano a loro volta il farmaco quando questo veniva somministrato ai loro cari con disturbi addominali e con diarrea che poi contraevano di conseguenza la SMON, causandosi inavvertitamente da soli la malattia che tanto temevano. Il risultato dell’epidemia in apparenza rese la SMON una malattia infettiva. In soldoni, quella che sembrava essere la cura per la SMON ne era in realtà la sua stessa causa.
I famigliari, dottori e infermieri, pensando di proteggersi, assumevano a loro volta il farmaco quando questo veniva somministrato ai loro cari con disturbi addominali e con diarrea che poi contraevano di conseguenza la SMON, causandosi inavvertitamente da soli la malattia che tanto temevano. Il risultato dell’epidemia in apparenza rese la SMON una malattia infettiva
Sono pochi i dottori a conoscenza della storia della SMON e forse sono ancora meno quelli che utilizzano lo slogan «cura o causa». Eppure oggi il fenomeno è più rilevante che mai. Uno studio pubblicato l’anno scorso sostiene l’ipotesi che oggi la terza causa di morte negli USA sia l’intervento medico, inclusi problemi legati ai farmaci soggetti a prescrizione e all’impianto di dispositivi medici, che vanno dallo stent cardiaco alla protesi dell’anca e ai dispositivi contraccettivi.
Si scoprì che il colore verde dell’urina del paziente era causato dalla dissoluzione del cliochinolo nel corpo dei pazienti.
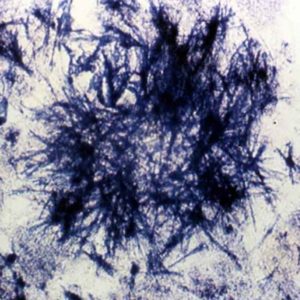
Il pigmento nell’urina di un paziente SMON è risultato essere il farmaco clioquinolo anti-diarrea, dissolto dal metabolismo del corpo
Gli esempi abbondano praticamente in tutte le specializzazioni, dalla cardiologia alla psichiatria e alla cura del cancro. Jerome Hoffman, professore emerito di medicina alla UCLA (University of California, Los Angeles), afferma che non è un fatto sorprendente: poiché i farmaci e i dispositivi medici puntano ai sistemi alterati del corpo, è molto facile sbagliare e peggiorare il disturbo.
In soldoni, quella che sembrava essere la cura per la SMON ne era in realtà la sua stessa causa.
Pochi dottori sono a conoscenza della SMON. Forse sono ancora meno quelli che usano lo slogan «cura o causa». Eppure oggi il fenomeno è più rilevante che mai.
Negli anni ‘80 e ‘90, per esempio, i pazienti venivano ampiamente curati con medicinali per il ritmo cardiaco in modo da evitare che i battiti irregolari, chiamati contrazioni ventricolari premature (CVP), scatenassero una fibrillazione ventricolare mortale.
Un farmaco può correggere le Contrazioni Premature Ventricolari ma uccidere il paziente: come un vecchio detto ricorda, l’operazione è riuscita
I medicinali andavano molto bene per ridurre i battiti irregolari e i dottori li avevano prescritti a molti credendo di salvare delle vite. Ma nel 1989, la sperimentazione clinica per la soppressione dell’aritmia cardiaca, in sigla CAST, sponsorizzata dagli Istituti Nazionali di Sanità, aveva dimostrato che, sebbene i medicinali annullavano effettivamente le CPV (Contrazioni Premature Ventricolari), quando queste comparivano, era molto più probabile che scatenassero fibrillazioni ventricolari mortali. I pazienti trattati avevano 3,6 volte la stessa possibilità di morire dei pazienti ai quali era stato somministrato un placebo.
Il farmaco può correggere le CPV ma uccidere il paziente: come un vecchio detto ricorda, l’operazione è riuscita, ma il paziente è deceduto. Il problema era rimasto invisibile per più di un decennio perché i dottori sostenevano che quando un paziente moriva improvvisamente fosse a causa delle condizioni del cuore e non per la cura che loro avevano prescritto.
Uno studio storico sul Prozac per curare la depressione negli adolescenti, aveva scoperto che in generale aumentava i comportamenti suicidi – mentre il suo reale compito era di prevenirli
In un altro caso di «cura o causa», uno studio storico sul Prozac per curare la depressione negli adolescenti, aveva scoperto che in generale aumentava i comportamenti suicidi – mentre il suo reale compito era di prevenirli. Nello studio, il 15% degli adolescenti depressi curati con il Prozac ha tentato il suicidio, contro il 6% curato con la psicoterapia e l’11% curato con farmaci placebo. Questi numeri non sono stati resi pubblici da Eli Lilly, il produttore, il ricercatore capo, che dichiarava che il Prozac fosse «il grande vincitore» tra i farmaci per la cura degli adolescenti depressi. I medici, ignari che il farmaco potesse aumentare il tasso di suicidi, spesso aumentavano il dosaggio quando i pazienti diventavano più depressi durante il trattamento, pensando che la causa fosse proprio la depressione e non la cura.
Ricerche condotte su altri farmaci della stessa classe del Prozac, inibitore selettivo della ricaptazione della serotonina, o SSRI, hanno mostrato problemi simili.
Vi sono molti altri casi del fenomeno «cura o causa»: stent cardiaci che hanno causato coaguli nelle arterie coronarie; defibrillatori-pacemaker impiantati che si sono inceppati o che hanno sbagliato ad attivarsi, causando ritmi cardiaci mortali; stimolatori del nervo vago per curare l’epilessia che hanno invece portato al suo aumento.
Vi sono molti altri casi del fenomeno «cura o causa»: stent cardiaci che hanno causato coaguli nelle arterie coronarie; defibrillatori-pacemaker impiantati che si sono inceppati o che hanno sbagliato ad attivarsi, causando ritmi cardiaci mortali; stimolatori del nervo vago per curare l’epilessia che hanno invece portato al suo aumento.
Una delle lezioni della SMON è il pericolo degli incentivi finanziari perversi. I medici giapponesi erano stati pagati per ogni prescrizione che facevano, una pratica considerata non etica nella maggior parte degli altri paesi. I medici, in alcune prefetture del Giappone, possono ancora vendere medicinali ai loro pazienti. Per forza prescrivevano così alte dosi di clioquinol per periodi prolungati.
Più della metà dei dottori negli Stati Uniti riceve somme di denaro o altri benefici dalla Big Pharma e dai produttori di dispositivi medici. Le cifre possono essere esorbitanti: alcuni dottori hanno ricevuto decine di milioni di dollari per impiantare certi dispositivi o per promuovere determinati farmaci.
Questa influenza ha però un costo sulle persone che sono esposte a trattamenti pericolosi. Un gruppo no profit, l’Institute for Safe Medication Practices, ha condotto uno studio per quantificare le conseguenze negative dei farmaci e ha concluso che i medicinali prescritti sono «uno dei pericoli più rilevanti per la salute dell’uomo che dipende dall’attività umana».
Una delle lezioni della SMON è il pericolo degli incentivi finanziari perversi. I medici giapponesi erano stati pagati per ogni prescrizione che facevano
Con l’aumento del complesso industriale-medico e i suoi ingenti profitti, il settore ha un interesse personale nell’incolpare la malattia del paziente per i risultati negativi e non i loro stessi prodotti.
Le affermazioni dell’industria farmaceutica spesso ingannano sia dottori che pazienti. Ciba-Geigy, il principale produttore del cliochinolo, affermava che il medicinale era sicuro perché non poteva essere assorbito nel sistema circolatorio dall’intestino. Eppure, le documentazioni di un caso contro l’azienda mostrano che Ciba-Geigy era consapevole da anni degli effetti pericolosi del farmaco.
Più della metà dei dottori negli Stati Uniti riceve somme di denaro o altri benefici dalla Big Pharma e dai produttori di dispositivi medici
All’inizio del 1944, gli inventori del cliochinolo dichiararono che il farmaco sarebbe dovuto essere rigidamente controllato e limitato a 10-14 giorni di somministrazione. Nel 1965, dopo che un veterinario svizzero pubblicò dei documenti in cui cani a cui era stato somministrato il clioochinolo avevano sviluppato attacchi epilettici e morirono, Ciba si era limitato a dichiarare che il farmaco non dovrebbe essere somministrato agli animali.
Con l’aumento del complesso industriale-medico e i suoi ingenti profitti, il settore ha un interesse personale nell’incolpare la malattia del paziente per i risultati negativi e non i loro stessi prodotti.
Negli Stati Uniti, l’influenza dell’industria farmaceutica su quello che i medici e il pubblico credono riguardo ai farmaci e ai dispositivi medici è scesa esponenzialmente, poiché quasi tutte le ricerche sono ora condotte dalle aziende e le ricerche effettivamente indipendenti non esistono più.
Nel 1997, la sponsorizzazione dell’industria ha fornito il 29% dei finanziamenti per ricerche cliniche e non cliniche. Le stime oggi affermano che la percentuale è aumentata a circa il 60%. Anche la ricerca «più indipendente», come quella condotta dagli Istituti Nazionali di Salute, è ora «associata» a un’azienda, rendendo la nostra dipendenza da loro quasi totale.
Arginare l’onda di interventi medici che possono provocare più danni che bene richiederà una profonda valutazione dei casi «cura o causa» – e la volontà di fermare la dipendenza da azienda farmaceutica che perversamente promuove.
Fonte: Undark

Big Pharma
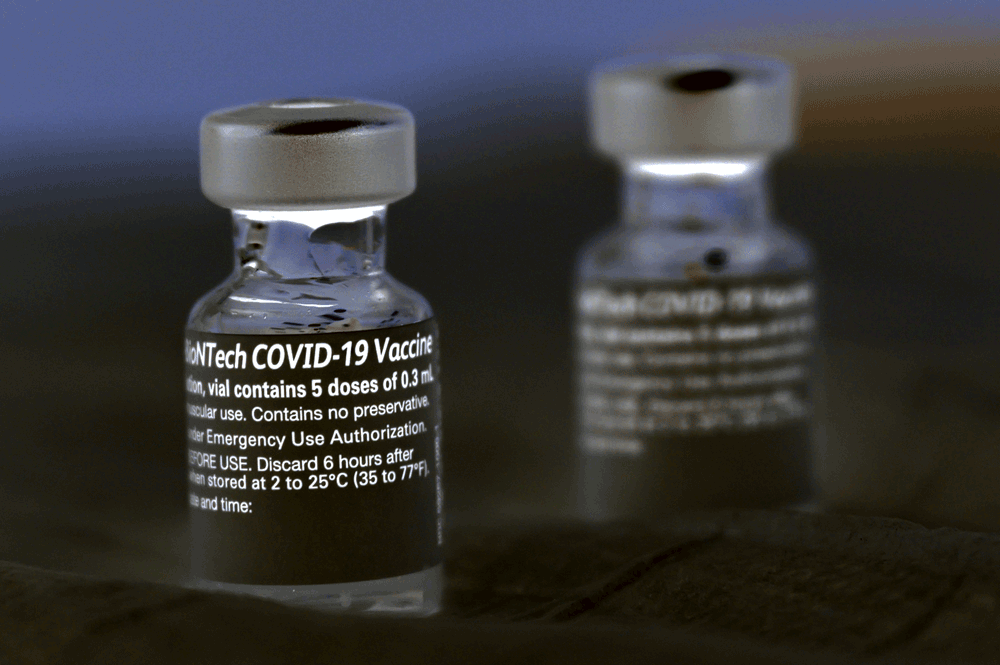
Affermazioni fuorvianti sul vaccino Pfizer «hanno portato discredito» a Big Pharma: parla un autorità di autoregolamentazione britannica
Renovatio 21 traduce questo articolo per gentile concessione di Children’s Health Defense. Le opinioni degli articoli pubblicati non coincidono necessariamente con quelle di Renovatio 21.
La Prescription Medicines Code of Practice Authority, un organismo indipendente e di autoregolamentazione istituito dall’Associazione dell’industria farmaceutica britannica, ha stabilito che l’azienda ha violato cinque regole del suo Codice di condotta per la pubblicità.
Un’agenzia di regolamentazione del Regno Unito ha scoperto che i migliori dipendenti Pfizer «hanno portato discredito» all’industria farmaceutica quando hanno fatto affermazioni fuorvianti che promuovevano un «medicinale senza licenza» nei tweet sul vaccino COVID-19, ha riferito domenica The Telegraph.
La Prescription Medicines Code of Practice Authority (PMCPA), un organismo indipendente e di autoregolamentazione istituito dall’Associazione dell’industria farmaceutica britannica, ha stabilito che l’azienda avrebbe violato cinque regole del suo Codice di condotta per la pubblicità.
L’organismo di vigilanza dell’industria farmaceutica britannica UsForThem ha presentato un reclamo al PMCPA nel febbraio 2023. Il reclamo riguardava i tweet del 2020 dei massimi dirigenti Pfizer, tra cui il direttore medico britannico Berkeley Phillips. I tweet erano ancora visibili sui social al momento della presentazione della denuncia.
Sostieni Renovatio 21
L’organizzazione ha affermato che Pfizer «ha promosso in modo fuorviante e illegale il suo vaccino contro il COVID-19» riportando tassi di efficacia relativa molto elevati senza fornire informazioni sui tassi di efficacia assoluta o informazioni richieste sulla sicurezza.
UsForThem ha affermato che era importante presentare questa denuncia due anni dopo perché «tale comportamento scorretto era ancora più diffuso» di quanto si pensasse in precedenza, estendendosi «fino ai vertici» delle attività di Pfizer nel Regno Unito e «apparentemente continuando fino ad oggi».
Commentando l’importanza dei risultati, Daniel O’Conner di Trial Site News, che ha anche trattato la storia, ha dichiarato a The Defender: «il comportamento di Pfizer durante la pandemia è stato davvero scandaloso. E ovviamente l’obiettivo: grandi soldi».
O’Connor ha affermato che il «comportamento aziendale di Pfizer durante la pandemia», come rivelato da questa e altre sentenze del PMCPA, è «altrettanto insidioso» quanto i problemi con i percorsi normativi per i farmaci e i principali difetti negli stessi studi clinici che Trial Site News ha monitorato.
Pfizer ha una chiara esperienza di agire come «impresa di profitto inaccettabile durante la peggiore pandemia del secolo», ha aggiunto. «La domanda che abbiamo è chi ha dato loro potere nel governo».
Grave censura per aver portato «discredito su» Big Pharma
La denuncia si concentrava su un tweet che Phillips di Pfizer ha condiviso su Twitter, ora X, originariamente realizzato da un dipendente Pfizer con sede negli Stati Uniti.
Il tweet affermava:
«Il nostro vaccino candidato è efficace al 95% nella prevenzione del COVID-19 e al 94% nelle persone di età superiore ai 65 anni. Archivieremo tutti i nostri dati presso le autorità sanitarie entro pochi giorni. Grazie a tutti i volontari della nostra sperimentazione e a tutti coloro che combattono instancabilmente questa pandemia».
Il comitato investigativo della PMCPA ha scoperto che quattro dipendenti di Pfizer UK avevano ritwittato il post e altri lo avevano messo «mi piace». Hanno detto che probabilmente il pubblico e gli operatori sanitari avrebbero visto il tweet.
Iscriviti alla Newslettera di Renovatio 21
La giuria ha concordato con le accuse di UsForThem secondo cui il messaggio conteneva informazioni limitate sull’efficacia e nessuna informazione sulla sicurezza, in violazione delle regole sull’inganno del pubblico e sulla fornitura di dati accurati sulla sicurezza.
Il panel ha inoltre sottolineato che i codici di condotta esistenti vietano la promozione dei medicinali prima della loro autorizzazione all’immissione in commercio. Tuttavia, in diretta violazione dei codici, i tweet dei dipendenti Pfizer hanno portato alla «diffusione proattiva di un farmaco senza licenza su Twitter agli operatori sanitari e al pubblico nel Regno Unito», ha rilevato la commissione.
I tweet violavano anche la politica stessa di Pfizer che vieta ai dipendenti Pfizer di interagire con i social media relativi ai medicinali e ai vaccini dell’azienda.
Il comitato PMCPA ha concluso che «Pfizer ha portato discredito e ridotto la fiducia nell’industria farmaceutica», il che, secondo lui, è una seria censura che riserva a gravi violazioni come quella in cui un’azienda ha promosso un farmaco prima ancora che fosse stato autorizzato.
I casi che si ritiene abbiano portato discredito all’industria vengono pubblicizzati sulla stampa medica, farmaceutica e infermieristica.
Un portavoce di Pfizer UK ha affermato che la società «riconosce e accetta pienamente le questioni evidenziate da questa sentenza PMCPA» e che è «profondamente dispiaciuta», secondo The Telegraph.
Pfizer ha inoltre affermato che esaminerà l’uso dei social media da parte dei propri dipendenti per garantire che rispettino i codici attuali e per prevenire tali problemi in futuro.
Il giornale ha anche riferito che Phillips, il cui re-tweet era principalmente in questione, ha affermato che il post era «accidentale e non intenzionale». «Detto questo, abbiamo immediatamente accettato la sentenza del caso e facciamo tutto il possibile per garantire che i nostri dipendenti aderiscano alla nostra rigorosa politica sui social media e al Codice di condotta del settore quando utilizzano i loro social media personali» ha aggiunto.
Altri cinque rimproveri legati alla promozione del vaccino anti-COVID
Pfizer è stata rimproverata sei volte dall’autorità di regolamentazione per la sua promozione non etica del vaccino COVID-19.
Il 4 marzo, pochi giorni dopo che la PMCPA aveva annunciato la sua sentenza sui tweet del 2020 che promuovevano il vaccino, l’agenzia ha anche annunciato una seconda sentenza , rilevando che Pfizer aveva violato un’altra clausola del codice di condotta in un tweet del 2022 di Pfizer UK che «non è riuscita a mantenere standard professionali».
Tale sentenza, emessa anche in risposta a una denuncia presentata da UsForThem, riguardava una serie di tre tweet pubblicati sul feed Twitter di Pfizer UK che includevano un collegamento a un articolo di Pulse Today.
Aiuta Renovatio 21
Quel tweet diceva:
«Mentre il Regno Unito entra nel suo primo «inverno sbloccato» dal 2019, il nostro [dichiarato dipendente medico senior di Pfizer] spiega l’impatto devastante che le malattie respiratorie possono avere durante i mesi più freddi. Leggi di più @PulseToday  #WinterPressures».
#WinterPressures».
Il tweet rimandava a un articolo promozionale — ripubblicato qui — commissionato da Pfizer su un sito web per operatori sanitari, ma non era chiaramente contrassegnato come contenuto promozionale pagato da Pfizer.
Il PMCPA in questo caso ha affermato di essere preoccupato che i tweet fossero disponibili al grande pubblico mentre il materiale nell’articolo di PulseToday era destinato agli operatori sanitari. Ciò ha violato gli elevati standard creati dai codici di condotta, hanno affermato le autorità di regolamentazione.
Nel febbraio 2023, l’agenzia ha scoperto che il CEO di Pfizer Albert Bourla, Ph.D., ha rilasciato commenti «fuorvianti» e «non qualificati» promuovendo l’uso dei vaccini mRNA contro il COVID-19 per i bambini piccoli durante un’intervista alla BBC.
In quel caso, UsForThem ha accusato il redattore medico della BBC, Fergus Walsh, di aver condotto l’intervista «come un’amichevole chiacchierata davanti al caminetto», dando a Bourla «un’opportunità promozionale gratuita che il denaro non può comprare» permettendogli di promuovere la diffusione del vaccino, in particolare tra i giovani. bambini per i quali il vaccino non era stato nemmeno autorizzato.
All’epoca, nessun vaccino contro il Covid-19 era stato approvato dall’Agenzia di regolamentazione dei medicinali e dei prodotti sanitari del Regno Unito per i bambini sotto i 12 anni, quindi la commissione ha ritenuto che i commenti di Bourla violassero il codice.
Due delle altre sentenze del PMCPA su Pfizer riguardavano i post di LinkedIn e una riguardava affermazioni fatte in un comunicato stampa.
La sanzione per la serie di violazioni, ha riferito The Telegraph, è una multa di 34.800 sterline.
Ben Kingsley, responsabile degli affari legali di UsForThem, ha dichiarato al Telegraph che «è sorprendente quante volte i dirigenti senior di Pfizer siano stati ritenuti colpevoli di gravi violazioni normative, in questo caso incluso il reato più grave di tutti ai sensi del Codice di condotta del Regno Unito».
«Tuttavia le conseguenze per Pfizer e le persone interessate continuano ad essere ridicole. Questo sistema di regolamentazione senza speranza per un’industria della vita e della morte multimiliardaria è diventato una farsa, che ha un disperato bisogno di riforme», ha affermato Kingsley.
«È assolutamente necessaria una radicale revisione del quadro normativo e legale in base al quale questo settore distrutto e corrotto può operare», ha twittato UsForThem.
I critici negli Stati Uniti hanno chiesto che i regolatori nazionali ritengano Pfizer responsabile in questo caso. In un tweet, Jay Bhattacharya, MD, Ph.D. di Stanford., ha invitato la Food and Drug Administration statunitense a farlo.
James Lyons-Weiler, Ph.D., ha scritto che la Federal Trade Commission e la Security and Exchange Commission intraprendono azioni simili.
Brenda Baletti
Ph.D.
©8 aprile 2024, Children’s Health Defense, Inc. Questo articolo è riprodotto e distribuito con il permesso di Children’s Health Defense, Inc. Vuoi saperne di più dalla Difesa della salute dei bambini? Iscriviti per ricevere gratuitamente notizie e aggiornamenti da Robert F. Kennedy, Jr. e la Difesa della salute dei bambini. La tua donazione ci aiuterà a supportare gli sforzi di CHD.
Renovatio 21 offre questa traduzione per dare una informazione a 360º. Ricordiamo che non tutto ciò che viene pubblicato sul sito di Renovatio 21 corrisponde alle nostre posizioni.
Iscriviti alla Newslettera di Renovatio 21
Immagine di U.S. Secretary of Defense via Wikimedia pubblicata su licenza Creative Commons Attribution 2.0 Generic; immagine modificata.
Alimentazione
Pfizer sospende la nuova pillola dimagrante dopo che i pazienti hanno riscontrato gravi effetti collaterali

Sostieni Renovatio 21
Aiuta Renovatio 21
Big Pharma
Sciroppo uccide i bambini usbechi. Dietro, un fiume di corruzione

Renovatio 21 pubblica questo articolo su gentile concessione di AsiaNews. Le opinioni degli articoli pubblicati non coincidono necessariamente con quelle di Renovatio 21.
Al processo per lo scandalo del Dok-1 Maks sta emergendo che i produttori indiani corrompevano regolarmente gli operatori sanitari in tutto il Paese, per raccomandare il preparato ai pazienti. Nel frattempo il presidente Mirziyoyev ha sostituito il ministro della Salute ma senza indicare quali nuove misure verranno adottate.
Il tribunale di Taškent ha ripreso le sessioni del processo sullo scandalo dello sciroppo Dok-1 Maks, la cui assunzione ha portato 18 bambini all’invalidità permanente, mentre in tutto le persone che hanno subito gravi conseguenze sono ormai una settantina. Sono stati aggiunti altri nomi alla lista delle persone accusate, che sono attualmente 23.
L’accusa evidenzia come dopo l’assunzione del farmaco 16 bambini abbiano ricevuti traumi molto seri, e tre siano morti direttamente dopo l’assunzione dello sciroppo.
Lo scorso agosto è divenuto evidente che il numero delle persone colpite dall’assunzione del farmaco della compagnia indiana Marion Biotech sia di molto superiore a quanto si supponesse. Se all’inizio del 2023 si parlava di una ventina di bambini coinvolti, oggi quelli accertati sono almeno 65, come ha riferito in tribunale l’ex-primario del centro plurifunzionale della regione di Samarcanda, il dottor Mamaktul Azizov.
Sostieni Renovatio 21
Il presidente del tribunale, Musa Jusipov, ha inserito nell’elenco degli accusati 17 persone, e nei prossimi giorni verranno esaminate tutte le rispettive posizioni. Secondo la Corte suprema dell’Uzbekistan, come pubblicato agli atti dello scorso 1° dicembre, una parte della documentazione è stata inviata agli organi inquirenti «per rivedere le conclusioni accusatorie e approfondire le azioni processuali integrative, relative al coinvolgimento di altre persone nello stato di accusa».
Finora gli accusati sono 21 persone, compreso l’ex-direttore dell’Agenzia per lo sviluppo farmaceutico e direttore della compagnia Quramax Medikal, un cittadino indiano, insieme a diversi altri a lui collegati, in tutto 16 uomini e 5 donne contro i quali sono state presentate le accuse da parte del Servizio per la sicurezza nazionale dell’SGB.
Alla compagnia sono state ritirate le licenze per il commercio di prodotti farmaceutici. La procura ha dichiarato che i distributori del Dok-1 Maks avevano pagato tangenti ai funzionari locali, nella misura di 33 mila dollari, per rinunciare alle verifiche obbligatorie del preparato da immettere sul mercato, che è stato così registrato come accessibile sul mercato interno dell’Uzbekistan.
Inoltre è stato chiarito che gli imprenditori indiani che hanno prodotto il mortale sciroppo corrompevano regolarmente gli operatori sanitari in tutto il Paese, per raccomandare il preparato ai pazienti.
Un rappresentante del comitato fiscale che ha testimoniato al processo ha spiegato che i produttori hanno pagato in tutto 5 miliardi e 57 milioni di som (circa mezzo milione di dollari) ai medici che raccomandavano lo sciroppo, e che aiutavano al suo acquisto. Le infermiere hanno ricevuto 122 milioni di som (circa 10 mila dollari), mentre i farmacisti hanno percepito 2 miliardi e 345 milioni di som (quasi 200 mila dollari). Oltre un milione di dollari è stato poi distribuito a vari altri collaboratori per la diffusione del farmaco.
L’anno scorso, secondo le informazioni diffuse da Radio Ozodlik, le autorità dello Stato indiano settentrionale dell’Uttar-Pradesh avevano autorizzato la Marion Biotech a rinnovare la produzione, ma dopo le morti di massa dei bambini in Uzbekistan lo sciroppo per la tosse è stato bloccato.
Nel frattempo, il presidente dell’Uzbekistan Šavkat Mirziyoyev ha sostituito il ministro della Salute, nominando come sostituto provvisorio Asilbek Khudajarov: in una riunione «in spirito critico» alla presenza del primo ministro Abdulla Aripov, è stato licenziato il ministro Amrillo Inojatov, senza ulteriori chiarimenti sui futuri programmi del ministero.
Invitiamo i lettori di Renovatio 21 a sostenere con una donazione AsiaNews e le sue campagne.
Renovatio 21 offre questo articolo per dare una informazione a 360º. Ricordiamo che non tutto ciò che viene pubblicato sul sito di Renovatio 21 corrisponde alle nostre posizioni.
Iscriviti alla Newslettera di Renovatio 21
-


 Spirito2 settimane fa
Spirito2 settimane faPapa Francesco attacca i non vaccinati, vescovo svizzero reagisce
-



 Occulto2 settimane fa
Occulto2 settimane faIl vescovo Strickland celebra una messa per contrastare l’attività satanica prevista durante l’eclissi solare
-



 Spirito2 settimane fa
Spirito2 settimane faRito catto-sciamanico in USA, «orrori liturgici abominevoli»: parla Mons. Viganò
-



 Pensiero4 giorni fa
Pensiero4 giorni faLa giovenca rossa dell’anticristo è arrivata a Gerusalemme
-



 Controllo delle nascite2 settimane fa
Controllo delle nascite2 settimane faOMS e riduzione della popolazione, cadono le maschere
-



 Civiltà1 settimana fa
Civiltà1 settimana faTutti contro lo spot con l’Eucarestia sostituita da una patatina. Ma il vero scandalo è il Concilio e la caduta della civiltà cristiana
-



 Scuola1 settimana fa
Scuola1 settimana faDal ricatto del vaccino genico alla scuola digitalizzata: intervento di Elisabetta Frezza al convegno su Guareschi
-



 Ambiente2 settimane fa
Ambiente2 settimane faTerremoto a Nuova York dopo che un fulmine ha colpito la Statua della libertà